A Kormány
a nemdohányzók védelméről és a dohánytermékek fogyasztásának, forgalmazásának egyes szabályairól szóló 1999. évi XLII. törvény 8. § (5) bekezdés a) pontjában,
a 12. § és a 24. § (2) bekezdés d) pontja tekintetében a nemdohányzók védelméről és a dohánytermékek fogyasztásának, forgalmazásának egyes szabályairól szóló 1999. évi XLII. törvény 8. § (5) bekezdés b) pontjában,
a 24. § (1) bekezdése és a 24. § (2) bekezdés c) pontja tekintetében az egészségügyi hatósági és igazgatási tevékenységről szóló 1991. évi XI. törvény 15. § (4) bekezdés a) pontjában,
a 24. § (2) bekezdés b) pontja tekintetében a jogalkotásról szóló 2010. évi CXXX. törvény 31. § (1) bekezdés a) pontjában
kapott felhatalmazás alapján, az Alaptörvény 15. cikk (1) bekezdésében meghatározott feladatkörében eljárva a következőket rendeli el:
1. § (1) * E rendelet rendelkezéseit – a (2) bekezdésben meghatározott kivétellel – a Magyarország területén előállított, továbbá – a 16. §-ban foglalt kivétellel – forgalomba hozott dohánytermékekre, elektronikus cigarettákra, utántöltő flakonra, dohányzást imitáló elektronikus eszközökre, nikotinmentes utántöltő flakonra és dohányzási célú gyógynövény termékekre, valamint a dohányzást helyettesítő nikotintartalmú termékekre kell alkalmazni.
(2) E rendelet rendelkezéseit nem kell alkalmazni a személyes fogyasztás céljából Magyarország területére behozott dohánytermékekre.
2. § * E rendelet alkalmazásában:
1. * bejegyzett kereskedő: a jövedéki adóról szóló törvény (a továbbiakban: Jöt.) szerinti bejegyzett kereskedő;
2. dohánytermék gyártásához felhasznált nyers- és adalékanyagok:
a) dohány: a dohánynövény levelei és más, feldolgozott vagy feldolgozatlan természetes részei, beleértve az expandált és a visszanyert dohányt is,
aa) nyersdohány: a Nicotiana tabacum fajhoz tartozó, ipari feldolgozásra alkalmas növény természetes vagy mesterséges úton szárított levele,
ab) fermentált, érlelt dohány: az a nyersdohány, amelyben a szárítást követően hőfejlődés és szárazanyag-veszteség mellett olyan változások játszódtak le, amelynek következtében a dohánytermék élvezeti célra alkalmassá vált,
b) dohányfólia: kötő- és adalékanyagok felhasználásával, szárazanyagra számítva legalább 75%-ban dohányból készült papírszerű lemez vagy szalag,
c) dohányvágat: egyenletes szélességű szálakra vágott dohány vagy egyenletes szélességűre vágott dohányfólia,
d) cigarettapapír: olyan méretre vágott, speciális papír, amit a dohányvágat burkolására használnak,
e) adalékanyag: a dohánytermékhez, annak csomagolási egységéhez vagy bármely gyűjtőcsomaghoz hozzáadott, dohánytól eltérő anyag;
3. dohányzásra szánt dohánytermék: a füst nélküli dohányterméktől eltérő dohánytermék, melynek típusai:
a) cigaretta: égési folyamat során fogyasztható dohányrúd, amely meglévő állapotában dohányzásra alkalmas, dohányvágatból vagy dohányvágatból és dohányfóliából készült töltetét hosszanti részén ragasztott cigarettapapír vagy dohányfólia borítja, és nem minősül szivarnak vagy szivarkának, továbbá az a dohányrúd, amelyet egy egyszerű, nem ipari eljárással cigarettapapír-hüvelybe tolnak vagy cigarettapapír-lappal körbevesznek,
b) szivar: égési folyamat során fogyasztható,
ba) természetes dohánylevelekből álló külső borítékkal rendelkező dohányrúd,
bb) a kocsányozott keverékdohányból készült szivarbélből, valamint a szivar szokásos színével megegyező színű, regenerált dohánylevélből készült, és a terméket – adott esetben a füstszűrőt is beleértve, a szopókával ellátott szivaroknál azonban a szopóka kivételével – teljesen körülölelő, külső borítékból álló dohányrúd, amely darabsúlya – füstszűrő vagy szopóka nélkül – legalább 2,3 gramm és legfeljebb 10 gramm, valamint amely hosszának legalább egyharmadánál mért kerülete eléri a 34 millimétert,
c) szivarka: legfeljebb 3 g súlyú szivar,
d) fogyasztási dohány: az e)–g) pont szerinti, további ipari feldolgozás nélkül dohányzásra alkalmas kész dohányvágat,
e) cigarettadohány (finomra vágott fogyasztási dohány): olyan dohány, amelyet a fogyasztók cigarettakészítésre használhatnak és amelyben a dohányrészecskék tömegének több mint 25%-a kisebb, mint 1,5 milliméter szélességűre vágott,
f) pipadohány (egyéb fogyasztási dohány): az e) pont hatálya alá nem tartozó, égési folyamat során fogyasztható dohány, amelyet kizárólag pipában történő elszívásra szántak,
g) vízipipadohány: olyan dohánytermék, amely vízipipával fogyasztható,
h) bármely olyan egyéb termék, amelyet dohányzás céljából gyártanak, még abban az esetben is, ha csupán részben tartalmaz – akár géntechnológiával módosított formában, akár nem ilyen formában – dohányt;
3a. * egészségvédő figyelmeztetés: a szöveges figyelmeztetés, a kombinált egészségvédő figyelmeztetés, az általános figyelmeztetés és a tájékoztatás;
4. export: olyan jövedéki terméknek az Európai Unión kívüli államba történő értékesítése, amelyet a vámhatóság végleges rendeltetéssel az Európai Unión kívüli államba kiléptet;
5. forgalomba hozatal: a termék – bármilyen módon történő – hozzáférhetővé tétele az unióbeli fogyasztók számára, tekintet nélkül a termék gyártásának helyére;
6. forgalomba hozó: az 5. pont szerinti tevékenységet végző gazdálkodó szervezet vagy természetes személy;
7. függőséget okozó tulajdonság: valamely anyag azon farmakológiai potenciálja, amellyel függőséget, vagyis olyan állapotot alakít ki, amely befolyásolja az egyén viselkedésének kontrollálására irányuló képességét, jellemzően valamilyen jutalom vagy a megvonási tünetek megszűnése következtében érzett megkönnyebbülés, illetve mindkettő által;
8. füst nélküli dohánytermék: olyan dohánytermék, amelynek a felhasználása nem jár égési folyamattal, beleértve a rágódohányt, a tüsszentésre szolgáló dohányterméket és a szájon át fogyasztott dohányterméket:
a) rágódohány: kizárólag rágásra szánt, füst nélküli dohánytermék,
b) tüsszentésre szolgáló dohánytermék: az orron át fogyasztható, füst nélküli dohánytermék,
c) * szájon át fogyasztott dohánytermék: a belélegzésre vagy rágásra szánt dohánytermékeken kívül minden szájon át való használatra szánt, teljes egészében vagy részben dohányból készült, porított vagy szemcsés, illetve e formák bármely kombinációja révén előállított dohánytermék, ideértve a zacskóban vagy likacsos szerkezetű zacskóban kiszerelt dohányterméket is;
9. füstszűrő: a cigaretta, szivar, szivarka azon része, amely a dohányterméken áthaladó főfüst szűrésére szolgál;
10. gyártó: az a természetes vagy jogi személy, amely terméket gyárt, illetve amely az adott terméket tervezteti vagy legyártatja, és a saját neve vagy kereskedelmi védjegye alatt forgalomba hozza;
11. idegen anyag: a termesztés és feldolgozás során a nyersanyagba, illetve a késztermékbe került, egyszerű fizikai módszerekkel elkülöníthető, nem dohány eredetű anyag;
12. * importálás: a Jöt. szerinti importálás;
13. * importáló: a Jöt. szerinti importáló;
14. ízesítés: illatot, ízt vagy illatot és ízt kölcsönző adalékanyag;
15. jellegzetes ízesítés: a dohánytól eltérő, adalékanyag vagy adalékanyagok kombinációjának használatából adódó, egyértelműen észlelhető – többek között gyümölcs, fűszer, gyógynövény, alkohol, cukorka, mentol vagy vanília – illat vagy íz, amely a dohánytermék fogyasztása előtt vagy során érzékelhető;
16. kátrány: a nikotinmentes száraz füst-kondenzátum;
17. kibocsátások: olyan anyagok, amelyek a dohánytermék vagy – a fiatalkorúak dohányzásának visszaszorításáról és a dohánytermékek kiskereskedelméről szóló 2012. évi CXXXIV. törvény 3. § 2. pontja szerinti – dohányterméket kiegészítő termék rendeltetésszerű felhasználása során szabadulnak fel, mint például a füstben előforduló anyagok vagy a füst nélküli dohánytermékek felhasználása során felszabaduló anyagok;
18. legmagasabb kibocsátási szint: egy adott anyagnak a dohánytermékben található, milligrammban mért maximális tartalma vagy kibocsátása (beleértve a nullát is);
19. nikotin: a nikotinalkaloid-tartalom;
20. nikotin tartalmú folyadék: az elektronikus cigaretta használata során felhasznált, illetve annak utántöltésére szolgáló folyadék, amely bármilyen kis mennyiségben nikotint tartalmaz;
21. összetevő: dohány, adalékanyag, valamint a kész dohánytermékben vagy kapcsolódó termékben jelen lévő anyagok vagy alkotóelemek, beleértve a papírt, a füstszűrőt, a nyomdafestéket, a kapszulákat és a ragasztóanyagokat is;
22. * szabadforgalomba bocsátás: a Jöt. szerinti szabadforgalomba bocsátás;
23. szállítási csomagolás: a termék szállításához kialakított, de kiskereskedelmi forgalomba nem kerülő csomagolás;
24. személyes fogyasztás: a dohánytermék nem kereskedelmi jelleggel, magánszemély által történő, a Jöt. szerinti adómentes behozatala;
25. szén-monoxid: a cigarettafüst gázfázisának alkotórésze;
26. szopóka: a cigarettához, szivarhoz, szivarkához, elektronikus cigarettához, dohányzást imitáló elektronikus eszközhöz rögzített rész, amely közvetlenül a szájjal érintkezik;
27. * adóraktár engedélyese: a Jöt. szerinti adóraktár engedélyese;
28. toxicitás: az adott anyag által az emberi szervezetben potenciálisan okozott káros hatás mértéke, beleértve a bizonyos idő bekövetkeztével, megismételt vagy folyamatos fogyasztás vagy expozíció folyamán okozott hatásokat;
29. új dohánytermék-kategóriák: olyan dohánytermék,
a) amely nem tartozik a következő kategóriák egyikébe sem: cigaretta, cigarettadohány, pipadohány, vízipipadohány, szivar, szivarka, rágódohány, tüsszentésre szolgáló dohánytermék vagy szájon át fogyasztott dohánytermék, és
b) amelyet 2014. május 19-e után hoznak forgalomba;
30. * hevített dohánytermék: olyan, az új dohánytermék-kategóriába tartozó termék, amelyet nikotin és más vegyi anyagok kibocsátása céljával hevítenek, amely kibocsátást a felhasználó belélegzi.
2/A. § * A 2. §-ban foglaltakon túl e rendelet alkalmazásában a nemdohányzók védelméről és a dohánytermékek fogyasztásának, forgalmazásának egyes szabályairól szóló 1999. évi XLII. törvény (a továbbiakban: Nvt.) 1. §-ában foglalt fogalom meghatározásokat kell figyelembe venni.
3. § (1) * Az adóraktár engedélyesének, az importálónak és a bejegyzett kereskedőnek a dohánytermék gyártásának megkezdése, illetve a dohánytermék szabad forgalomba bocsátása előtt valamennyi dohánytermékről az 1. mellékletben szereplő adatokat tartalmazó regisztrációs lapot kell kiállítania.
(2) * A regisztrációs lap egy példányát az adóraktárban, az importáló, a bejegyzett kereskedő székhelyén, illetve a raktározás helyén a hatósági ellenőrzés számára is hozzáférhető módon meg kell őrizni mindaddig, amíg a dohánytermék gyártása, importálása folyik, illetve a dohánytermék forgalomban van.
(3) * Az importáló, a bejegyzett kereskedő és az adóraktár engedélyese köteles a szabadforgalomba bocsátás előtt a regisztrációs lap egy további példányát nyilvántartásba vétel céljából a fogyasztóvédelemért felelős miniszternek megküldeni. A fogyasztóvédelemért felelős miniszter a nyilvántartásba vett regisztrációs lap másolati példányát elektronikus úton továbbítja a Nemzeti Népegészségügyi és Gyógyszerészeti Központ (a továbbiakban: NNGYK) részére.
(4) * Az 1. melléklet szerinti regisztrációs lap adattartalmáról a fogyasztóvédelemért felelős miniszter hatósági nyilvántartást vezet.
4. § * (1) A dohánytermék nem tartalmazhat idegen anyagokat.
(2) A dohánytermék nem tartalmazhat
a) vitaminokat vagy egyéb olyan adalékanyagokat, amelyek azt a benyomást keltik, hogy a dohányterméknek kedvező élettani hatása van, vagy az egészséget kevésbé veszélyezteti;
b) koffeint, taurint vagy egyéb olyan adalékanyagokat és élénkítő hatású vegyületeket, amelyekhez az energikusság és a vitalitás képzete társul;
c) a kibocsátásokat elszínező tulajdonságú adalékanyagokat;
d) a dohányzásra szánt dohánytermékek esetében az inhalációt vagy a nikotinfelvételt megkönnyítő adalékanyagokat;
e) az el nem égetett formában rákkeltő, mutagén vagy reprodukciót károsító tulajdonságokkal (a továbbiakban: CMR tulajdonság) rendelkező adalékanyagokat.
(3) A dohánytermék nem tartalmazhat a 4. melléklet szerinti tiltott adalékanyagokat.
(4) Tilos olyan dohánytermék forgalomba hozatala és forgalmazása, amely nem felel meg az (1)–(3) bekezdésben meghatározott követelményeknek.
(5) Az (1)–(4) bekezdésben foglaltakon túl tilos mentol, valamint mentolszármazék adalékanyagokat tartalmazó cigaretta és cigarettadohány forgalomba hozatala és forgalmazása.
(6) Az új adalékanyagoknak a dohánytermék gyártásában való felhasználását a felhasználás tervezett kezdő időpontját 6 hónappal megelőzően, de legkésőbb a felhasználás tervezett időpontját 30 nappal megelőzően a felhasználónak, a bejegyzett kereskedőnek, az importálónak vagy az adóraktár engedélyesének (a továbbiakban együtt: bejelentő) be kell jelentenie az NNGYK részére. A bejelentést a 3. melléklet szerinti adattartalommal kell megtenni. A bejelentett adatokról az NNGYK hatósági nyilvántartást vezet, és azt a honlapján közzéteszi. Nem szükséges bejelenteni a nyersdohány természetes részeinek felhasználását.
(7) A bejelentéshez mellékelni kell
a) az Európai Gazdasági Térségről szóló megállapodásban részes állam hatósága által kiadott felhasználási engedélyt, ha az rendelkezésre áll, és
b) az akkreditált laboratórium által kiadott, a bevizsgálás eredményét rögzítő jegyzőkönyvet.
(8) Az NNGYK a bejelentéstől számított 30 napon belül a bejelentés alapján megvizsgálja, hogy a felhasználni tervezett adalékanyag szerepel-e az e rendeletben tiltott adalékanyagok között. Amennyiben a vizsgálat során az NNGYK megállapítja, hogy a felhasználni tervezett adalékanyag használatát jogszabály nem tiltja, úgy a bejelentést tudomásul veszi, és erről tájékoztatja a bejelentőt. Az NNGYK a bejelentésről tájékoztatja a fogyasztóvédelemért felelős minisztert. Ha az NNGYK a 30 nap elteltével nem nyilatkozik, a bejelentett adalékanyag felhasználható.
(9) A (6) bekezdés szerint bejelentett adalékanyagokra vonatkozó tanulmányokat a felhasználás megkezdésétől számított 2 év elteltével a bejelentőnek meg kell küldenie az NNGYK részére. Az egészségügyért felelős miniszter által vezetett minisztérium a benyújtott dokumentáció alapján a benyújtástól számított 6 hónapon belül megvizsgálja, hogy a dokumentáció nem indokolja-e az adalékanyagnak a 4. melléklet szerinti tiltott adalékanyagok listáján történő szerepeltetését.
(10) Ha az országos tisztifőorvos úgy ítéli meg, hogy az adalékanyagot fel kell venni a 4. melléklet szerinti listára, úgy jogszabály-módosítást kezdeményez az egészségügyért felelős miniszternél a lista kibővítése érdekében.
(11) A bejelentett adalékanyagtól eltérő adalékanyag, továbbá a dohány-adalékanyagnak a bejelentésben meghatározott feltételektől eltérő alkalmazása tilos.
(12) A szabadforgalomba bocsátott cigarettának meg kell felelnie az MSZ EN 16156:2011 biztonsági követelményeinek.
(13) A határokon átnyúló távértékesítés esetében a dohányterméket abban a tagállamban forgalomba hozott dohányterméknek kell tekinteni, ahol a fogyasztó tartózkodik.
(14) E § alkalmazásában nem minősül új adalékanyagnak, és nem esik a (6) bekezdésben meghatározott bejelentési kötelezettség alá az az adalékanyag, amelyet a gyártó 2016. augusztus 20-át megelőzően jogszabályi felhatalmazás vagy külön engedély alapján használni volt jogosult a dohánytermék gyártásához, feltéve, hogy az nem szerepel a 4. melléklet szerinti tiltott adalékanyagok listáján.
4/A. § * (1) * A jellegzetes ízesítésű dohánytermékek forgalomba hozatala tilos, ide nem értve a dohánytermékek előállításához nélkülözhetetlen adalékanyagok – például az érlelési folyamat során elveszett cukortartalmat pótló cukor – használatát, ha az adalékanyagok nem eredményeznek jellegzetes ízesítésű terméket, és nem növelik jelentős vagy mérhető módon a dohánytermék függőséget okozó hatását, toxicitását, továbbá az el nem égett formában CMR tulajdonságait.
(2) Tilos az alkotóelemeikben – így a szűrőben, a papírban, a csomagolásban, a kapszulában, illetve az érintett dohánytermék illatát vagy ízét vagy füstintenzitásának megváltoztatását lehetővé tevő minden technikai megoldásban – ízesítést tartalmazó dohánytermékek forgalomba hozatala.
(3) A szűrő, a papír és a kapszula nem tartalmazhat dohányt vagy nikotint.
(4) Tilos az adalékanyagokat olyan mennyiségben tartalmazó dohánytermékek forgalomba hozatala, amelyek a fogyasztás szakaszában a dohánytermék mérgező vagy függőséget okozó hatását, vagy CMR tulajdonságait jelentős vagy mérhető módon megnövelik.
(5) * A cigarettától, a cigarettadohánytól és a hevített dohányterméktől eltérő dohánytermékek esetében az (1)–(3) bekezdésben foglalt tilalmak nem alkalmazandók.
5. § * (1) A szabadforgalomba bocsátott cigaretta legmagasabb kibocsátási szintje cigarettánként nem lehet több, mint: *
a) 10 mg kátrány,
b) 1 mg nikotin,
c) 10 mg szén-monoxid.
(2) A cigaretta kátránykibocsátását az MSZ ISO 4387, nikotinkibocsátását az MSZ ISO 10315, míg szén-monoxid-kibocsátását az MSZ ISO 8454 szabvány alapján kell mérni.
(3) A kátrány-, nikotin- és szén-monoxid-mérés pontosságát az MSZ ISO 8243 szabványnak megfelelően kell meghatározni.
(4) A (2) és (3) bekezdésben említett mérést az akkreditáló szervezet által engedélyezett és felügyelt laboratóriumokban kell hitelesíteni. A laboratóriumok nem lehetnek a dohányágazat közvetlen vagy közvetett tulajdonában, illetve nem állhatnak a közvetlen vagy közvetett ellenőrzése alatt.
(5) Az akkreditáló szervezet az általa engedélyezett laboratóriumok listáját, a laboratóriumok engedélyezése során alkalmazott kritériumokat, és a felügyelet módszereit az engedélyezést követő 30 napon belül megküldi az egészségügyért felelős miniszternek. Ha a megküldött adatokban változás áll be, az akkreditáló szervezet haladéktalanul értesíti az egészségügyért felelős minisztert.
(6) Az egészségügyért felelős miniszter a laboratóriumokkal kapcsolatosan rendelkezésére álló információkat továbbítja az Európai Bizottság részére. Az Európai Bizottság a jóváhagyott laboratóriumok listáját nyilvánosan hozzáférhetővé teszi.
6. § * (1) A csomagolási egységen jelölni kell
a) a dohánytermék típusát a következők szerint:
aa) „cigaretta”
ab) „szivar”
ac) „szivarka”
ad) „cigarettadohány”
ae) „pipadohány”
af) „rágódohány”
ag) „tüsszentésre szolgáló dohánytermék”
ah) „vízipipadohány”
ai) * „hevített dohánytermék”,
b) a dohánytermék márkanevét vagy márkajelzését,
c) a dohánytermék márkanevének vagy márkajelzésének alfajtáját (ha megkülönböztethető),
d) a gyártói vagy forgalmazói minőséget és a gyártó vagy forgalmazó cégjegyzék szerinti megnevezését,
e) a dohánytermék származási helyének megjelölését, ha az áru nem az Európai Gazdasági Térségből származik,
f) a darabszámot (cigaretta, szivar, szivarka esetén) vagy tömeget (fogyasztási dohány, rágásra, tüsszentésre szolgáló dohánytermék esetén),
g) füstszűrős termék esetén a „füstszűrő(s)” vagy „filter(es)” szót, és
h) a gyártás időpontját (az év, a hónap és a nap feltüntetésével) és helyét, vagy tételszámot, illetve kódolt megjelölést, amelyből a gyártás helye és ideje megállapítható.
(2) A gyűjtőcsomagon – az egészségvédő figyelmeztetésekre vonatkozó rendelkezéseken túl – az (1) bekezdés a)–f) pontja szerinti jelöléseket kell alkalmazni a csomagolási egységekre meghatározott feltételekkel.
(3) A szállítási csomagoláson az (1) bekezdés a)–f) pontja szerinti jelöléseket kell alkalmazni.
(4) A cigaretta csomagolási egysége kartonból vagy puha anyagból készülhet, és a felpattintható vagy felhajtható (flip-top) fedélen, illetve az oldalpántos doboz csapófedelén kívül nem lehet rajta olyan nyílás, amely az első felnyitás után újrazárható. A felpattintható vagy felhajtható (flip-top), illetve csapófedelű csomagolási egységek esetében a fedél csak a doboz hátsó oldalához rögzíthető. A cigaretta csomagolási egysége kizárólag téglatest alakú lehet.
(5) A cigarettadohány csomagolása téglalap alakú tasak vagy álló tasak lehet.
(6) Ha egy termék vízipipa útján és cigarettadohányként is használható, azt cigarettadohánynak kell tekinteni.
(7) Mentolos ízesítésű dohánytermék csomagolásán a mentol jelzése „mentol” felirattal történhet.
6/A. § * (1) Dohányzásra szánt dohányterméket forgalomba hozni csak abban az esetben lehet, ha annak minden csomagolási egysége és minden gyűjtőcsomagja – szembetűnően, kontrasztos háttérben, jól olvashatóan, eltávolíthatatlan nyomtatással, letörölhetetlenül, magyar nyelven – egyaránt tartalmazza
a) egyik oldalsó felületén, az oldal legalább 50%-át kitevő felületen az „A dohányzás halált okoz – szokjon le most!” általános figyelmeztetést,
b) másik oldalsó felületén, az oldal legalább 50%-át kitevő felületen az „A dohányfüst több mint 70 rákkeltő anyagot tartalmaz.” tájékoztatást, és
c) mindkét főoldalán, az oldal legalább 65%-át kitevő felületen az 5. mellékletben meghatározott lehetőségek közül a gyártó által választható kombinált egészségvédő figyelmeztetést.
(2) Az (1) bekezdés a) pontjában meghatározott általános figyelmeztetést a dohányterméket árusító üzlethelyiségben, illetve mozgó árusító hely kiszolgáló terében is el kell helyezni. A figyelmeztetés feltüntetésének módjára az (1) bekezdésben foglaltak megfelelően irányadóak azzal, hogy a figyelmeztető felirat legkisebb méretére vonatkozó rendelkezést nem kell alkalmazni.
(3) * A (2) bekezdésben meghatározott módon elhelyezett általános figyelmeztetés szövegét ki kell egészíteni a „Segítség a leszokáshoz: 06 80 200 493, www.leteszemacigit.hu” felirattal úgy, hogy a kibővített figyelmeztetés legkisebb felülete 420 × 594 mm legyen.
(4) * Az egészségvédő figyelmeztetések semmilyen módon nem takarhatják el, illetve nem szakíthatják meg a zárjegyeket, árcédulákat, az árukövetésre és nyomon követésre szolgáló jeleket vagy biztonsági elemeket a csomagolási egységeken.
(5) * Az egészségvédő figyelmeztetések nyomtatásának eltávolíthatatlannak, törölhetetlennek kell lennie a csomagolási egységeken és minden gyűjtőcsomagon, ideértve azt is, hogy azokat részben vagy egészen semmilyen formában nem takarhatja el, illetve nem zavarhatja meg semmilyen zárjegy, árcédula, biztonsági elem, csomagolóanyag, tasak, doboz vagy egyéb eszköz, amikor a dohánytermék forgalomba kerül. A cigarettától, valamint a cigarettadohánytól eltérő dohánytermékeken a feliratok és az egészségvédő figyelmeztetések a csomagra eltávolíthatatlanul rögzített matricán is elhelyezhetők.
(6) Az egészségvédő figyelmeztetéseknek a csomagon vagy gyűjtőcsomagon a számukra fenntartott teljes felületet el kell foglalniuk, és azokhoz nem lehet megjegyzést fűzni, azokat átfogalmazni vagy azokra bármely formában hivatkozni.
(7) Az egészségvédő figyelmeztetésnek a csomagolási egység kinyitásakor érintetlennek kell maradnia, kivéve a felpattintható vagy felhajtható (flip-top) fedelű dobozok esetében, amelyeken az egészségvédő figyelmeztetés a kinyitáskor megbontható ugyan, de csak oly módon, hogy a szöveg, a képek és a leszokással kapcsolatos információk grafikai egységessége és láthatósága megmaradjon.
(8) Az általános figyelmeztetést és a tájékoztatást fehér alapon, fekete színű, félkövér, Helvetica bold betűtípussal kell nyomtatni. A feliratot kisbetűvel kell szedni, kivéve a szöveg kezdőbetűjét, és azt az esetet, amikor a nagybetű használatát nyelvtani szabály követeli meg.
(9) Az egészségvédő figyelmeztetést 1 milliméter vastagságú fekete szegéllyel kell körülvenni az annak fenntartott felületen belül. A szegély semmilyen módon nem zavarhatja az egészségvédő figyelmeztetések szövegét. Az általános figyelmeztetést és a tájékoztatást a nyomtatására fenntartott területen középre zárva, míg a szöveges figyelmeztetést és a kombinált egészségvédő figyelmeztetést a csomag felső szélével párhuzamosan kell elhelyezni. Az általános figyelmeztetést és tájékoztatást – a fogyasztási dohányok tasakjai kivételével – a téglatest alakú csomagokon és minden gyűjtőcsomagon a csomagolási egység vagy gyűjtőcsomag oldalsó szélével párhuzamosan kell elhelyezni. Olyan betűméretet kell alkalmazni, amely biztosítja, hogy az egészségvédő figyelmeztetés szövege a rendelkezésre álló felület lehető legnagyobb hányadát foglalja el.
(10) A cigarettacsomagok és a cigarettadohányt tartalmazó gyűjtőcsomagok esetében az általános figyelmeztetést a csomagolások egyik oldalsó felületének alsó részén, a tájékoztatást a másik oldalsó felület alsó részén kell feltüntetni. A cigarettacsomagok csomagolási egysége, valamint a gyűjtőcsomagok esetében az általános figyelmeztetés és tájékoztatás szélességének legalább 20 mm-nek kell lennie, amelyet a csomagolási egység oldalsó felületének hosszabbik szélével párhuzamosan kell elhelyezni.
(11) A csapófedeles, oldalpántos doboz formájú csomagok esetében, amelyeknél az oldalsó felület két részre nyílik a csomag kinyitásakor, az általános figyelmeztetést és a tájékoztatást teljes egészében a két részre nyíló felület nagyobbik felén kell feltüntetni. Az általános figyelmeztetést a felső felületnek a doboz kinyitásakor látható belsején is fel kell tüntetni. Az ilyen típusú csomag oldalsó felületének legalább 16 mm magasnak kell lennie.
(12) A cigarettadohány esetében az általános figyelmeztetést és a tájékoztatást a 2015/1735 bizottsági végrehajtási határozat szerint azokon a felületeken kell feltüntetni, amelyekkel biztosítható, hogy az egészségvédő figyelmeztetés teljes egészében látható legyen.
(13) Az egészségvédő figyelmeztetések méretét a csomag zárt állapotában az adott felület alapján kell kiszámítani.
6/B. § * (1) * A 2. § 3. pont a) és e) alpontjában meghatározott dohánytermékek csomagolásán kizárólag a 6. §-ban, valamint a 6/A. §-ban vagy jogszabályban, továbbá az Európai Unió kötelező jogi aktusában meghatározott elemeket lehet feltüntetni, azzal, hogy a 6. §, valamint a 6/A. § rendelkezéseit a (2)–(12) bekezdésben foglalt eltérésekkel kell alkalmazni.
(2) Cigarettát és cigarettadohányt forgalomba hozni a (3)–(12) bekezdésben foglalt feltételekkel lehet.
(3) A cigaretta és a cigarettadohány
a) minden csomagolási egységének és minden gyűjtőcsomagjának külső felülete a FORMULA GUIDE/solid matte színskálában PANTONE 448 M színű, matt felületű, a csomagoló-alapanyag matt, fehér színű,
b) minden csomagolási egységének és minden gyűjtőcsomagjának belső felülete megegyezik a csomagoló-alapanyag matt, fehér színével, kivéve a cigarettadohány csomagolási egysége esetében a csomagolás belső, átlátszó, festetlen fóliája,
c) csomagolási egységének és gyűjtőcsomagjának külső felülete nem tartalmazhat díszítő mélyedéseket, dombornyomást vagy egyéb díszítő elemeket,
d) csomagolási egysége és gyűjtőcsomagja nem tartalmazhat színezett vagy nem átlátszó ragasztóanyagot,
e) csomagolási egysége és gyűjtőcsomagja nem tartalmazhat az Nvt. 6/A. §-ában meghatározott rendelkezésektől eltérő bármely, a csomagolásba behelyezett vagy ahhoz hozzáerősített elemet, és
f) a 6. § (1) bekezdés b) és c) pontja tekintetében a csomagolási egység, illetve a gyűjtőcsomag kizárólag a következőket tartalmazhatja:
fa) a márka nevét, és
fb) az adott cigaretta, cigarettadohány márkajelzés alfajtájának nevét.
(4) A (3) bekezdés f) pontja szerinti jelöléseknek a következő feltételeknek kell megfelelniük:
a) színe a FORMULA GUIDE/solid matte színskálában PANTONE Cool Gray 1 M,
b) a márka neve, valamint az adott cigaretta, illetve cigarettadohány alfajtájának neve kizárólag egy-egy sort foglalhat el,
c) az adott cigaretta, illetve cigarettadohány alfajtájának neve közvetlenül a márka neve alatt szerepelhet,
d) a márka neve, valamint az adott cigaretta, illetve cigarettadohány alfajtájának neve Helvetica betűtípussal szerepelhet,
e) a márka neve legfeljebb 14 pontos betűméretű lehet,
f) az adott cigaretta, illetve cigarettadohány alfajtájának neve legfeljebb 10 pontos betűméretű lehet,
g) a szó első karakterét kivéve minden karaktert kisbetűvel kell feltüntetni, és
h) a megjelenítés semmilyen módon nem takarhatja el a csomagolási egységen található egészségvédő figyelmeztetéseket, és azok megjelenítését nem zavarhatja.
(5) A cigaretta minden csomagolási egységének és minden gyűjtőcsomagjának a csomagolására nyomtatott, a (3) bekezdés f) pontja szerinti márkanévnek, valamint a márkajelzés alfajtájának a következő feltételeknek kell megfelelnie:
a) azt a csomagolás elülső főoldalának és a csomagolás tetejének külső felületén kell elhelyezni – az elülső főoldalon az egészségvédő figyelmeztetés alatt – középre rendezve, és
b) az az elülső főoldalon, illetve a csomagolás tetején is csak egyszer szerepelhet.
(6) A cigarettadohány minden csomagolási egységének és minden gyűjtőcsomagjának a csomagolására nyomtatott, a (3) bekezdés f) pontja szerinti márkanévnek, valamint a márkajelzés alfajtájának a következő feltételeknek kell megfelelnie:
a) azt a csomagolás két főoldalának külső felületén kell elhelyezni, az egészségvédő figyelmeztetés alatt vagy mellett középre rendezve, és
b) az mind a két főoldalon csak egyszer szerepelhet.
(7) Ha a cigaretta csomagolása bélést is tartalmaz, a bélés:
a) matt fehér vagy matt ezüst színű lehet,
b) nem rendelkezhet díszítő bemélyedésekkel, dombornyomással vagy egyéb díszítő elemekkel, ide nem értve a csomagológépen alkalmazott, a teljes felületre felvitt, nem díszítési célú érdesítést,
c) nem tartalmazhat színezett vagy nem átlátszó ragasztóanyagot, és
d) nem tartalmazhat az Nvt. 6/A. §-ában meghatározott rendelkezésektől eltérő bármely, a csomagoláshoz hozzáerősített elemet.
(8) A cigaretta és a cigarettadohány – a gyűjtőcsomagnak vagy szállítási csomagolásnak nem minősülő – fedő csomagolóanyagának vagy külső csomagolása bármely egyéb formájának a következő feltételeknek kell megfelelnie:
a) átlátszó,
b) nem színezett,
c) nem rendelkezhet díszítő bemélyedésekkel, dombornyomással vagy egyéb díszítő elemekkel,
d) nem rendelkezhet jelzéssel vagy védjeggyel, a meghatározott előírásokkal összhangban lévő, tépőcsíktól eltérő elemmel,
e) nem tartalmazhat színezett vagy nem átlátszó ragasztóanyagot, és
f) nem tartalmazhat az Nvt. 6/A. §-ában meghatározott rendelkezésektől eltérő bármely, a csomagoláshoz hozzáerősített elemet.
(9) A cigaretta és a cigarettadohány csomagolóanyagán elhelyezett tépőcsíknak a következő feltételeknek kell megfelelnie:
a) átlátszó,
b) nem rendelkezhet díszítő bemélyedésekkel, dombornyomással vagy egyéb díszítő elemekkel,
c) nem rendelkezhet márkajelzéssel vagy jelzéssel,
d) nem tartalmazhat az Nvt. 6/A. §-ában meghatározott rendelkezésektől eltérő bármely, a csomagoláshoz hozzáerősített elemet,
e) nem tartalmazhat színezett vagy nem átlátszó ragasztóanyagot,
f) egyetlen folytonos és állandó szélességű vonalból állhat, és
g) a felhajtható felső fedélhez a lehető legközelebb a fedéllel párhuzamosan kell elhelyezni.
(10) Az (1)–(9) bekezdésben foglaltakat nem kell alkalmazni:
a) az egészségvédő figyelmeztetésekre,
b) az Nvt.-ben előírt egyéb elemekre, és
c) * a zárjegyre.
(11) Az (1)–(10) bekezdésben foglaltaktól eltérően a csomagolási egység alsó vagy egyik oldalsó felületén és gyűjtőcsomagján fel lehet tüntetni az értékesítést, illetve a külön jogszabály szerinti nyomon követést szolgáló vonalkódot vagy technikai jelet.
(12) Az (1)–(11) bekezdésben foglaltakat a Magyarország területén értékesítésre szánt cigaretták és cigarettadohányok csomagolásán kell alkalmazni.
6/C. § * (1) A csomagolási egységben található cigarettaszálaknak a következő feltételeknek kell megfelelniük:
a) a külső felületükön nem tartalmazhatnak díszítő mélyedéseket, dombornyomást vagy egyéb díszítő elemeket,
b) nem tartalmazhatnak színezett vagy nem átlátszó ragasztóanyagot,
c) nem tartalmazhatnak az Nvt.-ben előírtaktól eltérő elemet,
d) a cigarettát fedő papír fehér színű, és
e) a cigaretta füstszűrővel rendelkezik, azzal, hogy
ea) a füstszűrő látható része fehér színű, és
eb) a cigarettapapír füstszűrőt fedő része fehér színű vagy parafa utánzatú.
(2) A csomagolási egységben található szálankénti cigarettára nyomtatott szöveg a következőket tartalmazhatja:
a) a márka nevét, és
b) az adott cigaretta alfajtájának nevét.
(3) A (2) bekezdés szerinti feliratnak a következő feltételeknek kell megfelelnie:
a) a FORMULA GUIDE/solid matte színskálán PANTONE 444 M színű,
b) a márka nevét, illetve az adott cigaretta alfajtáját a dohányrúdon úgy lehet szerepeltetni, hogy az a füstszűrő végződéséhez a lehető legközelebb helyezkedjen el és körkörösen szerepeljen rajta,
c) a márka neve, illetve az adott cigaretta alfajta csak egyszer tüntethető fel és csak egy-egy sort foglalhat el,
d) az adott cigaretta alfajta neve közvetlenül a márka neve alatt szerepelhet,
e) a szó első karakterét kivéve minden karaktert kisbetűvel kell feltüntetni, és
f) a márka neve, valamint az adott cigaretta alfajtájának neve Helvetica betűtípusú lehet.
6/D. § * (1) A 2. § 3. pont a), e) és g) alpontjában meghatározott dohánytermékektől eltérő dohányzásra szánt dohánytermék esetében a 6/A. § rendelkezéseit a (2)–(10) bekezdésben foglalt eltérésekkel kell alkalmazni.
(2) A 2. § 3. pont a), e) és g) alpontjában meghatározott dohánytermékektől eltérő dohányzásra szánt dohánytermékek esetében a 6/A. § (1) bekezdése szerinti egészségvédő figyelmeztetések közül kizárólag
a) * a 6/A. § (1) bekezdés a) pontja szerinti általános figyelmeztetést kell feltüntetni az egyik főoldal legalább 30%-át kitevő felületen, a főoldal alsó részén a következő szöveggel: „A dohányzás halált okoz – szokjon le most! Segítség a leszokáshoz: 06 80 200 493, www.leteszemacigit.hu”, és
b) a 6/A. § (1) bekezdés c) pontja szerinti kombinált egészségvédő figyelmeztetést kell feltüntetni a másik főoldal legalább 40%-át kitevő felületen, a főoldal alsó részén.
(3) A (2) bekezdés b) pontja szerinti, az 5. mellékletnek megfelelően három csoportra osztott kombinált egészségvédő figyelmeztetéseket a rendszeres megjelenés biztosítása érdekében úgy kell alkalmazni, hogy egy csoport egy adott évben használható, és a csoportok évente váltakoznak.
(4) Az általános figyelmeztetést 3 milliméternél nem vékonyabb és 4 milliméternél nem vastagabb fekete szegéllyel kell körülvenni. Ennek a szegélynek az általános figyelmeztetés számára fenntartott felületen kívül kell elhelyezkednie.
(5) A 2. § 3. pont a), e) és g) alpontjában meghatározott dohánytermékektől eltérő dohányzásra szánt dohánytermékek esetében a 6/A. § (8) bekezdésében foglaltakat a (2) bekezdés a) pontjában foglalt általános figyelmeztetésre kell alkalmazni.
(6) A 2. § 3. pont a), e) és g) alpontjában meghatározott dohánytermékektől eltérő dohányzásra szánt dohánytermékek esetében a (2) bekezdés a) pontjában foglalt általános figyelmeztetést a nyomtatására fenntartott területen középre zárva, míg a kombinált egészségvédő figyelmeztetést a csomag felső szélével párhuzamosan kell elhelyezni. A nyomtatásra fenntartott felület a csomagolás adott oldalának közepétől eltérő helyen is elhelyezhető.
(7) A (2) bekezdés szerinti egészségvédő figyelmeztetések nyomtatásakor olyan betűméretet kell alkalmazni, amely biztosítja, hogy az egészségvédő figyelmeztetés szövege a rendelkezésre álló felület lehető legnagyobb hányadát foglalja el.
(8) A 2. § 3. pont a), e) és g) alpontjában meghatározott dohánytermékektől eltérő dohányzásra szánt dohánytermékekre a 6/A. § (10) bekezdése és a 7. § (2) bekezdése nem alkalmazandó.
(9) A 2. § 3. pont c) alpontjában meghatározott dohánytermékre a 6/A. § (11) bekezdése nem alkalmazandó.
(10) A 2. § 3. pont f) alpontjában meghatározott dohánytermék esetén az általános figyelmeztetés és a kombinált egészségvédő figyelmeztetés – ha a dohánytermék hátsó főoldalán kerül feltüntetésre – a főoldal felső részén, a csomagon található többi információval azonos irányban is felhelyezhető.
6/E. § * (1) A füst nélküli dohánytermékek valamennyi csomagolási egységén és minden gyűjtőcsomagján fel kell tüntetni a következő egészségvédő figyelmeztetést: „Ez a dohánytermék károsítja az Ön egészségét és függőséghez vezet.”
(2) Az (1) bekezdésben említett egészségvédő figyelmeztetésnek meg kell felelnie a 6/A. § (9) és (10) bekezdésében foglalt követelményeknek. Az egészségvédő figyelmeztetés szövegének párhuzamosnak kell lennie az e figyelmeztetések számára fenntartott felületen található fő szöveggel, valamint
a) azt a csomagolási egység és minden gyűjtőcsomag két legnagyobb felületén kell feltüntetni, és
b) a csomagolási egység és minden gyűjtőcsomag megfelelő felületének 30%-át kell kitöltenie.
(3) * E § rendelkezéseit alkalmazni kell a hevített dohánytermékre is.
6/F. § * (1) A dohányzási célú gyógynövénytermékek valamennyi csomagolási egységének és bármely gyűjtőcsomagjának elülső és hátsó külső felületén fel kell tüntetni a következő egészségvédő figyelmeztetést: „E termék dohányzási célú fogyasztása károsítja egészségét.”
(2) Az egészségvédő figyelmeztetésnek meg kell felelnie a 6/A. § (9) és (10) bekezdésében foglalt követelményeknek. A figyelmeztetésnek a csomagolási egység és bármely gyűjtőcsomag megfelelő felületén a felület 30%-át kell kitöltenie.
(3) A dohányzási célú gyógynövénytermékek csomagolási egységei és gyűjtőcsomagjai nem tartalmazhatnak olyan elemet vagy megoldást, amely
a) * azt annak jellemzői, egészséghatásai, veszélyei vagy a kibocsátások tekintetében téves benyomást keltő módon reklámozza, illetve ilyen módon annak fogyasztására ösztönöz, a címkék nem tartalmazhatnak a termék nikotin-, kátrány- és szén-monoxid-tartalmára vonatkozó információt,
b) * azt sugallja, hogy egy adott termék kevésbé káros, mint más termékek, vagy a füst egyes káros összetevői hatásának csökkentését célozza, vagy annak vitalizáló, energizáló, gyógyító, fiatalító, természetes, organikus jellemzői vannak, vagy más egészség- vagy életmódbeli előnyökkel jár, vagy
c) ízre, illatra, ízesítőanyagra vagy más adalékanyagra, illetve ezek hiányára a fogyasztók megtévesztésére alkalmas módon utal.
(4) A (3) bekezdésben foglaltakon túl a dohányzási célú gyógynövénytermékek csomagolási egységein és gyűjtőcsomagjain nem tüntethető fel az az állítás, miszerint a termék ízesítő- és adalékanyagoktól mentes.
6/G. § * (1) A dohánytermékek minden csomagolási egységét egyedi azonosítóval kell megjelölni. Az egyedi azonosító sértetlenségének biztosítása érdekében azt eltávolíthatatlanul kell nyomtatni vagy rögzíteni, annak kitörölhetetlennek kell lennie, és azt semmilyen módon nem lehet eltakarni vagy megszakítani például zárjegyek vagy árcédulák által, illetve a csomagolási egység felnyitásakor.
(2) Az egyedi azonosítónak lehetővé kell tennie a következők meghatározását:
a) a gyártás helye és időpontja,
b) a gyártó létesítmény,
c) a dohánytermék gyártásához használt gép,
d) a gyártási műszak vagy a gyártás időpontja,
e) a termék leírása,
f) a kiskereskedelmi értékesítés célpiaca,
g) a tervezett szállítási útvonal,
h) adott esetben az európai uniós importőr,
i) a tényleges szállítási útvonal a gyártástól az első kiskereskedelmi egységhez, beleértve valamennyi igénybe vett raktárt, valamint a szállítás időpontját, a szállítás rendeltetési helyét, a kiindulási helyet és a címzettet,
j) a gyártástól az első kiskereskedelmi egységig valamennyi vásárló azonosítása és
k) a gyártástól az első kiskereskedelmi egységig valamennyi vásárló számlái, megrendelési számai és kifizetési bizonylatai.
(3) A (2) bekezdés a), b), c), d), e), f), g) és adott esetben h) pontja szerinti információk az egyedi azonosító részét képezik.
(4) A (2) bekezdés i), j) és k) pontja szerinti információk az egyedi azonosítóhoz vezető linken keresztül elektronikusan hozzáférhetők a jogszabályban meghatározottak szerint.
(5) A dohánytermékek kereskedelmében részt vevő valamennyi gazdasági szereplő – a gyártótól kezdve az első kiskereskedelmi egység előtti utolsó gazdasági szereplőig – köteles nyilvántartást vezetni a birtokába kerülő összes csomagolási egységről, valamint a csomagolási egységek minden közbenső mozgásáról és a birtokából való végleges kikerülésükről. Ez a kötelezettség teljesíthető gyűjtőcsomagolások – például karton, mesterkarton vagy raklap – megjelölésével és nyilvántartásával is, feltéve, hogy így is lehetséges minden csomagolási egység árukövetése és nyomon követése.
(6) A dohánytermékek ellátási láncában részt vevő valamennyi természetes és jogi személy köteles teljes körű és pontos nyilvántartást vezetni valamennyi vonatkozó ügyletről.
(7) A dohánytermékek gyártói kötelesek a dohánytermékek kereskedelmében részt vevő valamennyi gazdasági szereplő – a gyártótól kezdve az első kiskereskedelmi egység előtti utolsó gazdasági szereplőig, ideértve az importőröket, raktárakat és szállítási vállalatokat – rendelkezésére bocsátani a megvásárolt, eladott, tárolt, szállított vagy más módon kezelt dohánytermékek nyilvántartását lehetővé tevő eszközöket. Az eszköznek képesnek kell lennie a rögzített adatok elektronikus úton történő olvasására és azoknak a (8) bekezdés szerinti adattároló rendszerhez való továbbítására.
(8) A dohánytermékek gyártói és importőrei kötelesek egy független harmadik féllel adattárolási szerződést kötni tárhely biztosítása céljából valamennyi vonatkozó adat tárolásához. Az adattároló rendszert fizikailag az Európai Unió területén kell elhelyezni. A harmadik fél alkalmasságát, különösen annak függetlenségét és technikai felkészültségét, valamint az adattárolási szerződést az Európai Bizottság hagyja jóvá.
(9) A (8) bekezdés szerinti harmadik személy tevékenységét a dohánytermék gyártója által ajánlott és fizetett, az Európai Bizottság által jóváhagyott külső ellenőr ellenőrzi. A külső ellenőrnek éves jelentést kell benyújtania a vámhatóság és az Európai Bizottság részére, amelyben különösen a hozzáféréssel kapcsolatos szabálytalanságokat értékeli.
(10) * Az adattároló rendszerhez teljes hozzáférhetőségre jogosult a vámhatóság, a Szabályozott Tevékenységek Felügyeleti Hatósága, az Európai Bizottság és a külső ellenőr. Kellően indokolt esetben a vámhatóság a gyártók vagy importőrök számára hozzáférést biztosít ezekhez a tárolt adatokhoz, feltéve, hogy a kereskedelmi szempontból érzékeny információk továbbra is a vonatkozó jogszabályok által előírt megfelelő védelemben részesülnek.
(11) A rögzített adatokat a dohánytermékek kereskedelmében részt vevő gazdasági szereplő nem módosíthatja vagy törölheti.
6/H. § * (1) A dohánytermékek minden forgalomba hozott csomagolási egysége látható és nem látható elemekből álló, a termék bontatlanságát biztosító biztonsági elemet tartalmaz, amelynek a segítségével megállapítható, hogy a termék eredeti-e. A biztonsági elemet eltávolíthatatlan módon kell nyomtatni vagy rögzíteni, annak letörölhetetlennek kell lennie, és az semmilyen módon nem takarható el vagy szakítható meg például zárjegyek, árcédulák vagy más, jogszabályban előírt elemek által.
(2) Az (1) bekezdés szerinti biztonsági elemet a Jöt. szerinti dohánytermék zárjegy tartalmazza.
7. § * (1) * A 2. § 3. pont a), e) és g) alpontjában meghatározott dohányzásra szánt dohánytermékeken kombinált egészségvédő figyelmezetést kell feltüntetni. A kombinált egészségvédő figyelmezetésnek
a) a csomagolási egység mind elülső, mind hátsó oldala külső felületének, valamint minden gyűjtőcsomag mind elülső, mind hátsó oldala külső felületének 65%-át ki kell töltenie,
b) ugyanazt a szöveges figyelmeztetést és a kapcsolódó színes fényképet a csomagolási egység és valamennyi gyűjtőcsomag mindkét oldalán meg kell jelenítenie, azzal, hogy a gyűjtőcsomagon alkalmazott szöveges figyelmeztetéstől és a kapcsolódó színes fényképtől az adott gyűjtőcsomagon belül található csomagolási egységeken alkalmazott szöveges figyelmeztetés és a kapcsolódó színes fénykép eltérhet,
c) a csomagolási egység, illetve minden gyűjtőcsomag felső szélén kell elhelyezkednie, ugyanabban az irányban, mint a csomag azon felületén megjelenő bármely más információ, és
d) a cigaretta csomagolási egységei esetében a következő méretűnek kell lennie:
da) magasság: legalább 44 mm,
db) szélesség: legalább 52 mm.
(2) A kombinált egészségvédő figyelmeztetések fölé márkanév és – ha az feltüntethető – logó abban az esetben sem helyezhető, ha a 21/A. § (13) bekezdése szerint megengedett eltérés alapján a kombinált egészségvédő figyelmeztetéseket 2019. május 20-áig nem a csomagolás felső szélén helyezik el.
8. § * (1) Az 5. mellékletnek megfelelően három csoportra osztott kombinált egészségvédő figyelmeztetéseket a rendszeres megjelenés biztosítása érdekében dohánytermék márkanevenként úgy kell alkalmazni, hogy egy csoport egy adott évben használható és a csoportok évente váltakoznak.
(2) Dohánytermék márkanevenként, ha egy adott évben az adott termék gyártása szünetel, akkor a következő gyártás során a következő csoportba tartozó kombinált figyelmeztetéseket kell alkalmazni.
(3) Egy adott évben, dohánytermék márkanevenként az adott évben használt csoportba tartozó kombinált egészségvédő figyelmeztetések azonos arányban alkalmazandók.
(4) * Ha a (3) bekezdésben foglalt rendelkezés betartásának műszaki feltételei nem adottak, a leggyakrabban és a legritkábban alkalmazott kombinált egészségvédő figyelmeztetések száma közötti eltérés naptári évenként nem lehet nagyobb cigaretta esetében 10%-nál, egyéb dohánytermék-típus esetében 15%-nál. A kombinált egészségvédő figyelmeztetések váltakozva való alkalmazását előíró kötelezettség ellenőrizhetősége érdekében az importáló, a bejegyzett kereskedő és az adóraktár engedélyese köteles olyan nyilvántartást vezetni, amelyből az alkalmazott kombinált egészségvédő figyelmeztetések száma három hónaponként megállapítható.
9. § * (1) A kombinált egészségvédő figyelmeztetés
a) a dohánytermék csomagolásán akként kerül nyomtatásra, hogy – a (3) bekezdésben foglaltakra is figyelemmel – megtartsa az 5. melléklet szerinti formátumot és arányokat, valamint a kép és a szöveg grafikai sértetlenségét,
b) betölti a számára előírt felszín teljes egészét, valamint a csomagolás felső szélével párhuzamosan és a csomagon található többi információval azonos irányban helyezkedik el, és
c) sokszorosítása során a nyomtatásra a 6. mellékletben meghatározott műszaki előírásokat kell alkalmazni.
(2) A dohánytermék csomagolásán semmilyen formában nem lehet a kombinált egészségvédő figyelmeztetésekre megjegyzést tenni, azokat átfogalmazni vagy azokra utalni.
(3) * Az (1) bekezdés a) pontjában foglaltaktól eltérően, olyan dohánytermékek esetében, amelyek egyedi csomagolásának méretarányaira tekintettel, vagy a 6/D. § (2) bekezdés b) pontjában meghatározott 40%-os felületi lefedettség alkalmazása mellett nem lehetséges az előírt felület lefedése a kombinált egészségvédő figyelmeztetés 5. melléklet szerinti formátumának, arányainak vagy a kép és a szöveg grafikai sértetlenségének megváltoztatása nélkül, a kombinált egészségvédő figyelmeztetés az egyedi csomagolás méretéhez, illetve a 6/D. § (2) bekezdés b) pontjában meghatározott 40%-os felületi lefedettséghez történő igazítással a 6. melléklet 2. pontjában meghatározott előírások szerint alkalmazandó.
(4) * A (3) bekezdés alkalmazásának elősegítése érdekében a fogyasztóvédelemért felelős miniszter a honlapján közzéteszi az Európai Bizottság által e tárgyban kiadott útmutatót.
(5) A kombinált egészségvédő figyelmeztetéseket
a) úgy kell nyomtatni, hogy azokat ne takarja el vagy ne zavarja meg a csomag kibontása, és
b) olyan módon kell elhelyezni, amely biztosítja, hogy a csomag felbontásakor a kombinált figyelmeztetések egyetlen szöveges vagy vizuális eleme se csorbuljon.
(6) * A kombinált egészségvédő figyelmeztetések nyomdai kivitelezésére alkalmas elektronikus forrásdokumentumokat az NNGYK kérelemre elektronikus úton átadja a dohánytermék gyártója részére.
10. § *
11. § * (1) A dohányzási korlátozással érintett, valamint a dohányzásra kijelölt helyeket, helyiségeket, közterületeket, valamint a nemdohányzó intézményeket a 7. mellékletben meghatározott tartalmú és formájú felirat vagy jelzés alkalmazásával kell megjelölni. A felirat vagy jelzés mérete legalább A/4-es nagyságú. A feliraton vagy jelzésen szereplő „DOHÁNYZÁSRA KIJELÖLT HELY” és „TILOS A DOHÁNYZÁS” szövegeknek piros színnel, legalább 30 pontos Helvetica Bold, az egyéb szövegrészeknek legalább 18 pontos Helvetica Bold betűmérettel kell készülniük.
(1a) * Az (1) bekezdés szerinti felirat vagy jelzés alatt az elektronikus cigaretta és a dohányzást imitáló elektronikus eszköz használatának korlátozását, valamint használatára kijelölt helyeket, helyiségeket, közterületeket is érteni kell.
(2) * A népegészségügyi feladatkörében eljáró járási (fővárosi kerületi) hivatal kérelemre, a kérelmező részére engedélyezi az (1) bekezdésben és a 7. mellékletben foglaltaktól eltérő felirat vagy jelzés alkalmazását, ha *
a) a kérelmező által egyidejűleg az Nvt. 2. § (7) bekezdése és az (1) bekezdés alapján alkalmazandó jelzések száma a tízet meghaladja,
b) az (1) bekezdés és a 7. melléklet szerinti formájú felirat vagy jelzés alkalmazása a kérelmező számára műszaki vagy gazdasági okokból aránytalan nehézséggel járna, és a kérelmező által javasolt forma alkalmazása a kérelmező méltányolható érdekét szolgálja,
c) a kérelmező által engedélyeztetni kívánt felirat vagy jelzés adattartalma a 7. mellékletben foglaltakkal megegyező, és annál kevesebb adatot nem tartalmaz,
d) az engedélyeztetni kívánt felirat vagy jelzés felszíne legalább 62 370 négyzetmilliméter és
e) az alkalmazott betűk mérete nem kisebb az (1) bekezdésben meghatározott betűméretnél.
(3) A (2) bekezdés szerinti engedély iránti kérelemhez mellékelni kell az engedélyeztetni kért felirat vagy jelzés grafikai tervét, valamint tervezett elhelyezésének részletes leírását.
(4) * A népegészségügyi feladatkörében eljáró járási (fővárosi kerületi) hivatal a (2) bekezdés szerinti kérelmezőkről nyilvántartást vezet, a kérelmezők és az engedélyt kapók listáját évente, március 31-éig elektronikus úton megküldi az NNGYK részére.
12. § (1) * Az egészségvédelmi bírságot a bírságot kiszabó népegészségügyi feladatkörében eljáró fővárosi és vármegyei kormányhivatal a 8. mellékletben meghatározott számlájára kell befizetni.
(1a) * Az egészségvédelmi bírság összege
a) a dohányzással összefüggő tilalmak, korlátozások megsértése esetén legalább 20 000, legfeljebb 50 000 forint;
b) a dohányzóhelyek kijelölésére vonatkozó kötelezettség nem vagy nem megfelelő teljesítése, valamint a dohányzást érintő tilalmak, korlátozások megtartására vonatkozó ellenőrzési kötelezettség elmulasztása esetén, továbbá a dohányzási korlátozással érintett, valamint a dohányzásra kijelölt helyeken, helyiségekben, valamint közterületeken nem, vagy nem megfelelő felirat vagy más egyértelmű jelzés alkalmazása esetén, illetve annak nem szembetűnő módon történő megjelölése esetén
ba) * legalább 100 000, legfeljebb 250 000 forint a rendelkezésre jogosult tekintetében, illetve
bb) legalább 1 000 000, legfeljebb 2 500 000 forint az intézmény, szervezet, üzemeltető vagy gazdasági társaság tekintetében.
(1b) * A kiszabott egészségvédelmi bírság összegét úgy kell meghatározni, hogy az igazodjék a cselekmény súlyához és az elkövető személyi körülményeihez. Az eljáró hatóság az (1a) bekezdés a) pontja szerinti esetben – az ott meghatározott összeghatártól eltérően – a törvénysértőt 30 000 forintig terjedő helyszínen kiszabott egészségvédelmi bírsággal sújthatja. A helyszínen kiszabott bírság 30 napon belül történő meg nem fizetése esetén az (1a) bekezdést kell alkalmazni.
(2) * A népegészségügyi feladatkörében eljáró vármegyei és a fővárosi kormányhivatal és a népegészségügyi feladatkörében eljáró járási (fővárosi kerületi) hivatal az általa az adott hónapban az Nvt. alapján kiszabott egészségvédelmi bírság összegéről nyilvántartást vezet. A nyilvántartás személyazonosításra alkalmatlan, összesített adattartalmáról, valamint a tárgyhónapban bekövetkezett változásairól népegészségügyi feladatkörében eljáró fővárosi és a vármegyei kormányhivatal a tárgyhónapot követő hónap 20. napjáig elektronikus úton tájékoztatja az NNGYK-t.
(3) * Az (1) és (2) bekezdésben foglaltaktól eltérően, ha egészségügyi államigazgatási szervként a rendvédelmi szervek, a Magyar Honvédség, a Katonai Nemzetbiztonsági Szolgálat, az Országgyűlési Őrség, valamint a honvédelemért felelős miniszter tulajdonosi joggyakorlása alatt álló gazdasági társaságok közegészségügyi-járványügyi feladatait ellátó egyes szervek kijelöléséről szóló kormányrendeletben meghatározott elsőfokú közegészségügyi-járványügyi hatósági jogkör gyakorlója járt el,
a) az egészségvédelmi bírságot a 8/A. mellékletben meghatározott szervnek az ott megjelölt, központosított beszedési célelszámolási számlájára kell befizetni,
b) a (2) bekezdés szerinti nyilvántartási és tájékoztatási kötelezettséget az elsőfokú közegészségügyi-járványügyi hatósági jogkör gyakorlója teljesíti.
(4) * Az Nvt. rendelkezéseinek betartásával kapcsolatban beérkező lakossági észrevételek rögzítésére szolgáló 06 80 200 493 számú telefonvonal, illetve a www.leteszemacigit.hu honlap – amelyek az 5. és a 7. mellékletnek, továbbá az Nvt. 6. § (3) bekezdésének megfelelő helyen is feltüntetésre kerülnek – működtetése és a beérkezett információk feldolgozása az egészségügyért felelős miniszter által vezetett minisztérium hatáskörébe tartozik.
13. § (1) Csak olyan dohánytermék bocsátható szabadforgalomba, illetve hozható forgalomba, amely megfelel e rendelet előírásainak és a regisztrációs lapon feltüntetett adatoknak.
(2) Szájon át fogyasztott dohánytermék nem bocsátható szabadforgalomba, illetve nem hozható forgalomba.
(3) * A dohánytermék gyártásával összefüggésben, forgalomba hozatala során vagy forgalomba hozatalával összefüggésben nem adható át olyan termék, különösen kiegészítő csomagolás, doboz vagy tasak, amely a zárjegy vagy az egészségvédő figyelmeztetések vagy a kombinált figyelmeztetések eltakarására alkalmas.
14. § A dohánytermék minőségének megőrzéséhez szükséges tárolási körülményeket a forgalomba hozatal valamennyi szakaszában biztosítani kell. A szállítási csomagoláshoz használt gyűjtőládát legalább 10 cm magasságú, légkicserélődést elősegítő alátéten kell tárolni. A tárolási körülményeket, azoknak a dohánytermékek minőségére gyakorolt hatását a forgalomba hozó köteles rendszeresen ellenőrizni.
15. § Dohánytermék – a darabonként értékesíthetők kivételével – csak eredeti fogyasztói csomagolási egységben vagy gyűjtőcsomagban hozható forgalomba. A dohánytermék a forgalomba hozatal során nem csomagolható át, a gyűjtőcsomag olyan felbontását kivéve, amely a fogyasztói csomagolási egységekre való szétválasztást eredményezi. A fogyasztói csomagolási egység nem bontható meg.
15/A. § * A csomagolási egység
a) * cigaretta esetében 20 db cigarettát tartalmazó csomag,
b) a 2. § 3. pont b) pont ba) alpontja és a 2. § 3. pont b) pont bb) alpontja esetén
ba) szivarkának nem minősülő szivar esetén darab vagy doboz,
bb) szivarka esetén legalább 5 darabot tartalmazó doboz,
c) * a fogyasztási dohány esetében a legalább 30 gramm, de legfeljebb 50 gramm – de minden esetben maradék nélkül tízzel osztható grammtömegű – fogyasztási dohányt tartalmazó téglalap alakú vagy álló tasak, azzal, hogy vízipipadohány esetében a legfeljebb 50 gramm vízipipadohányt tartalmazó doboz is,
d) rágásra szolgáló vagy tüsszentésre szolgáló dohánytermékek esetében tasak vagy doboz.
16. § A Magyarországon export és az Európai Unió más tagállamába történő értékesítés céljára előállított dohányterméknek az 5. §-ban meghatározott előírásoknak kell megfelelnie.
17. § (1) * Az e rendeletben foglaltak betartását
a) * a 4. § szerinti bejelentés, valamint – ide nem értve a termékek csomagolási egységeire vonatkozó előírásokat – a 9/B. alcím tekintetében az országos tisztifőorvos,
b) a 11. §-ban foglaltak tekintetében a népegészségügyi feladatkörében eljáró járási (fővárosi kerületi) hivatal,
c) a 9/A. alcím tekintetében – ide nem értve a termékek csomagolási egységeire vonatkozó előírásokat – a gyógyszerészeti államigazgatási szerv,
d) az a)–c) pontban nem említett rendelkezések tekintetében a fogyasztóvédelmi hatóság
ellenőrzi, és hatáskörében eljár az e rendeletben foglaltak megsértése esetén.
(2) * A dohánytermékeknek a regisztrációs lap adatainak való megfeleléséért az importáló, a bejegyzett kereskedő és az adóraktár engedélyese felelős. Az importáló, a bejegyzett kereskedő és az adóraktár engedélyese a szükséges vizsgálatokat saját laboratóriurnában végezheti, vagy más, erre az országos tisztifőorvos által kijelölt laboratóriumban végeztetheti.
(3) A cigaretta kátrány-, nikotin- és szén-monoxid hozamának értékeit a fogyasztóvédelmi hatóság vizsgálja és igazolja. A vizsgálat és igazolás kiállításának költsége a vizsgálatot, illetve igazolás kiállítását kérő gyártót, importálót vagy a bejegyzett kereskedőt terheli.
(4) * A fogyasztóvédelemért felelős miniszter éves jelentésben megadja az egészségügyért felelős miniszter, az agrárpolitikáért felelős miniszter és az élelmiszerlánc-felügyeletért felelős miniszter részére az előállított dohánytermékek (3) bekezdés alapján mért adatait a kátrány, nikotin és szén-monoxid tekintetében.
(5) * Bármely, az Európai Gazdasági Térségről szóló megállapodásban részes állam hatáskörrel rendelkező hatósága által akkreditált laboratórium is jogosult a cigaretta kátrány, nikotin és szén-monoxid hozama értékeinek vizsgálatára és igazolására. A laboratóriumok nem lehetnek a dohányágazat közvetlen vagy közvetett tulajdonában, illetve nem állhatnak a közvetlen vagy közvetett ellenőrzése alatt.
(6) E rendelet előírásainak alkalmazása szempontjából a 9. mellékletben felsorolt szabványok irányadóak.
(7) * Cigaretta esetében a regisztrációs lapon közölt füstadatok értékfeltüntetésének megfelelőségét az MSZ ISO 8243 szabvány szerint kell igazolni.
18. § * (1) A dohánytermék forgalomba hozatalát megelőzően azok gyártójának és importálójának be kell nyújtania a 2015/2186 bizottsági végrehajtási határozat szerinti közös adatbeviteli kapun keresztül márkanevenként és alfajtánként magyar vagy angol nyelven
a) a dohánytermékek összetevőire vonatkozó adatokat az egyes összetevők súlyának csökkenő sorrendjében, és
b) a dohánytermékeknek az 5. § (1) bekezdése szerinti kibocsátási szintekre, valamint az ezeken túli kibocsátásokra vonatkozó adatait.
(2) A dohánytermék forgalomba hozatalát megelőzően azok gyártójának és importálójának évente március 31-éig be kell nyújtania a dohánytermékek értékesítési volumenére vonatkozó adatokat a 2015/2186 bizottsági végrehajtási határozat szerinti közös adatbeviteli kapun keresztül márkanevenként és alfajtánként magyar vagy angol nyelven. A tárgyév a listák benyújtását megelőző év január 1-jétől december 31-éig tart.
(3) Az (1) bekezdés szerint benyújtott adatokat a forgalomba hozatalt megelőzően ismételten be kell nyújtani, ha valamely termék összetétele akként módosul, hogy az befolyásolja a szolgáltatott információkat.
(4) * Az (1) bekezdés a) pontja szerinti adatszolgáltatás mellett meg kell indokolni, hogy miért kell az egyes összetevőket az adott dohánytermékekbe elegyíteni, továbbá meg kell adni az összetevők státuszát – beleértve azt, hogy regisztrálták-e – és típusát. A felsoroláshoz mellékelni kell az összetevőknek az elégetett vagy el nem égetett formáira vonatkozó mindazon toxikológiai adatokat is, amelyek az importáló, a bejegyzett kereskedő és az adóraktár engedélyese rendelkezésére állnak, különös tekintettel azoknak az emberi egészségre gyakorolt hatására, figyelemmel többek között a függőség kialakulásának veszélyére. Cigaretta és cigarettadohány esetében a gyártónak vagy az importálónak a felhasznált adalékanyagokat és tulajdonságaikat általánosan ismertető technikai dokumentumot is be kell nyújtania.
(5) A kátrányra, a nikotinra és a szén-monoxidra vonatkozó adatok kivételével a gyártóknak és az importálóknak meg kell adniuk az alkalmazott kibocsátásmérési módszereket. A gyártóknak és az importálóknak el kell végezniük a fogyasztóvédelemért felelős miniszter által meghatározott vizsgálatokat annak érdekében, hogy értékeljék az összetevőknek az egészségre gyakorolt hatását, figyelembe véve többek között függőséget okozó tulajdonságukat és toxicitásukat.
(6) A dohánytermékek gyártójának és importálójának évente, március 31-éig a dohánytermékekre vonatkozó információk benyújtása és nyilvános hozzáférhetővé tétele céljából be kell nyújtania a piackutatásra és a különböző fogyasztói csoportok – beleértve a fiatalokat és az aktív dohányosokat – preferenciáira vonatkozó, az összetevőkkel és a kibocsátásokkal kapcsolatos, rendelkezésre álló belső és külső tanulmányokat, valamint az új termékek bevezetése előtt végzett piackutatásai összefoglalóit, valamint az új termékek bevezetése előtt végzett piackutatások összefoglalóit. Az információk benyújtása a közös adatbeviteli kapun keresztül, elektronikus formában történik. Az információkat magyar vagy angol nyelven kell szolgáltatni.
(7) * A közös adatbeviteli kapun keresztül feltöltött adatokat az agrárpolitikáért felelős miniszter minden év április 30-áig, az üzleti titok védelmére tekintettel, az általa vezetett minisztérium honlapján keresztül nyilvánosságra hozza, és elektronikus formában megküldi az egészségügyért felelős miniszter és az NNGYK részére.
18/A. § * (1) A 18. § (1) bekezdése szerinti adatszolgáltatáson túl a dohánytermék gyártójának és importálójának az Európai Bizottság végrehajtási rendeletében meghatározott prioritási listán szereplő adalékanyagok tekintetében fokozott jelentéstételi kötelezettsége van.
(2) Az (1) bekezdés szerinti jelentéstételi kötelezettség keretében a dohánytermékek gyártójának és importálójának átfogó tanulmányokat kell végeznie, amelyekben minden egyes érintett adalékanyag vonatkozásában meg kell vizsgálni, hogy az adalékanyag
a) hozzájárul-e az érintett termékek toxicitásához vagy függőséget okozó tulajdonságához, valamint hogy az adalékanyag hatása következtében növekszik-e jelentős vagy mérhető mértékben bármely érintett termék toxicitása vagy függőséget okozó tulajdonsága,
b) eredményez-e jellegzetes ízt,
c) elősegíti-e az inhalációt vagy a nikotinfelvételt, vagy
d) hatására keletkeznek-e CMR tulajdonságokkal rendelkező anyagok, valamint ezek mennyiségét, továbbá azt, hogy az adalékanyag hatása következtében fokozódik-e jelentős vagy mérhető mértékben bármely érintett termék CMR tulajdonsága.
(3) A (2) bekezdés szerinti tanulmányokban figyelembe kell venni az érintett termékek rendeltetését, és meg kell vizsgálni különösen az érintett adalékanyag jelenléte mellett lezajló égési folyamat során keletkező kibocsátásokat. A tanulmányokban továbbá azt is meg kell vizsgálni, hogy milyen interakció alakul ki az összetevő és az érintett termékekben megtalálható egyéb összetevők között. A dohánytermékeikben ugyanazt az adalékanyagot használó gyártók vagy importálók végezhetnek közös vizsgálatot abban az esetben, ha a szóban forgó adalékanyagot hasonló termékösszetételben alkalmazzák.
(4) * A (2) és (3) bekezdés alapján készített tanulmányokról a gyártóknak vagy importálóknak jelentést kell készíteniük, melyben fel kell tüntetni a tanulmányok összefoglalóját, valamint átfogó áttekintést a szóban forgó adalékanyagról megjelent tudományos publikációkról és az adott adalékanyag hatásaira vonatkozó belső adatokról. Az így elkészített jelentést a gyártóknak vagy az importálóknak – legkésőbb 18 hónappal azt követően, hogy a szóban forgó adalékanyag felkerült a prioritási listára – be kell nyújtaniuk az Európai Bizottsághoz, valamint annak egy példányát meg kell küldeniük az NNGYK-nak.
(5) * Az Európai Bizottság és az NNGYK a gyártóktól vagy az importálóktól kiegészítő információt kérhet a szóban forgó adalékanyagról. Ez a kiegészítő információ a jelentés részét képezi.
(6) * Ha az országos tisztifőorvos az e § szerinti jelentés alapján szükségesnek ítéli meg, úgy a prioritási listán szereplő adalékanyagok további felhasználásának megtiltása érdekében jogszabály-módosítást kezdeményez az egészségügyért felelős miniszternél.
18/B. § * (1) * A dohánytermékek gyártói, importálói és a bejegyzett kereskedők kötelesek bejelenteni, ha új dohánytermék-kategóriákba tartozó dohányterméket kívánnak forgalomba hozni. A bejelentést az agrárpolitikáért felelős miniszter, az élelmiszerlánc-felügyeletért felelős miniszter, az egészségügyért felelős miniszter és az NNGYK számára elektronikus formában kell benyújtani, hat hónappal a tervezett forgalomba hozatalt megelőzően. A bejelentéshez mellékelni kell az érintett új dohánytermék részletes leírását és egy használati útmutatót, valamint információkat kell szolgáltatni a termék összetevőiről és kibocsátásairól a 2015/2186 bizottsági végrehajtási határozat szerinti adattartalommal.
(2) Az új dohánytermék-kategóriákról bejelentést benyújtó gyártóknak, importálóknak és bejegyzett kereskedőknek az (1) bekezdésben megjelöltek részére a következőket is be kell nyújtaniuk:
a) a rendelkezésre álló tudományos tanulmányok az új dohánytermék toxicitásáról, függőséget okozó tulajdonságáról és vonzerejéről,
b) a rendelkezésre álló tanulmányok, azok összefoglalói és piackutatások különböző fogyasztói csoportok, köztük a fiatalok és az aktív dohányosok preferenciáiról, és
c) egyéb rendelkezésre álló és lényeges információk, ideértve a termék kockázat/haszon elemzését, a dohányzásról való leszokásra, a dohányzás elkezdésére és előre jelzett fogyasztói megítélésre gyakorolt várható hatásait.
(3) Az új dohánytermék-kategóriákba tartozó dohánytermékek gyártói, importálói és bejegyzett kereskedői kötelesek az (1) bekezdésben megjelöltek részére benyújtani minden, a (2) bekezdés a)–c) pontjában említett tanulmánnyal vagy egyéb információval kapcsolatos új vagy frissített információt. Az új dohánytermék-kategóriákba tartozó dohánytermékek gyártói, importálói és bejegyzett kereskedői további vizsgálatok elvégzésére vagy további információk benyújtására is kötelezhetőek.
(4) * Az egészségügyért felelős miniszter a szolgáltatott adatok és információk alapján megítéli, hogy szükséges-e a termék betiltása.
(5) Az e §-ban foglaltak alapján kapott információkat az agrárpolitikáért felelős miniszter megküldi az Európai Bizottságnak.
18/C. § * (1) A dohányzási célú gyógynövénytermék a következő feltételekkel hozható forgalomba és forgalmazható:
a) nem tartalmazhat a 4. melléklet szerinti adalékanyagot,
b) nem tartalmazhat hozzáadott vitaminokat vagy egyéb olyan adalékanyagokat, amelyek azt a benyomást keltik, hogy a terméknek kedvező élettani hatása van, vagy az egészséget kevésbé veszélyezteti,
c) nem tartalmazhat hozzáadott koffeint, hozzáadott taurint vagy egyéb olyan adalékanyagokat és élénkítő hatású vegyületeket, amelyekhez az energikusság és a vitalitás képzete társul,
d) az inhalációt megkönnyítő adalékanyagokat és
e) CMR tulajdonságokkal rendelkező adalékanyagokat.
(2) Az (1) bekezdéstől eltérően azon dohányzási célú gyógynövénytermékek tekintetében, amelyek fogyasztása hevítéssel történik,
a) az (1) bekezdés a) pontjában foglalt rendelkezés akként alkalmazandó, hogy e termék teát tartalmazhat;
b) az (1) bekezdés b)–d) pontjában foglalt anyagok annyiban felhasználhatóak, amennyiben azok a növény, gyógynövény vagy gyümölcs, illetve a hozzáadott ízesítőanyag nélkülözhetetlen alkotóelemei.
(3) A dohányzási célú gyógynövénytermékek gyártója, importálója vagy forgalmazója köteles bejelenteni, ha dohányzási célú gyógynövényterméket kíván forgalomba hozni. A bejelentést az agrárpolitikáért felelős miniszter, az egészségügyért felelős miniszter és az országos tisztifőorvos számára elektronikus formában kell benyújtani, hat hónappal a tervezett forgalomba hozatalt megelőzően. A bejelentéshez mellékelni kell az érintett dohányzási célú gyógynövénytermék részletes leírását, valamint információkat kell szolgáltatni a termék gyártásában felhasznált valamennyi összetevőről és azok mennyiségéről, márkanevenként és alfajtánként.
(4) A dohányzási célú gyógynövénytermék gyártója vagy importálója köteles továbbá a (3) bekezdésben megjelölt szerveket tájékoztatni, ha valamely termék összetétele úgy módosul, hogy az befolyásolja az e § szerint szolgáltatott információkat. A dohányzási célú gyógynövénytermék gyártója vagy importálója további vizsgálatok elvégzésére vagy további információk benyújtására is kötelezhető.
(5) A dohányzási célú gyógynövénytermékekre vonatkozó bejelentések vizsgálata során az országos tisztifőorvos a fiatalkorúak dohányzásának visszaszorításáról és a dohánytermékek kiskereskedelméről szóló törvényben foglaltak figyelembevételével, a szolgáltatott adatok és információk alapján megítéli, hogy szükséges-e a termék betiltása. Az országos tisztifőorvos a dohányzási célú gyógynövénytermékekre vonatkozó bejelentések vizsgálatát követően – amennyiben a termék betiltása nem szükséges – a benyújtást követő 60 napon belül igazolást állít ki. Ha az országos tisztifőorvos 60 napon belül nem nyilatkozik, úgy a bejelentett termék forgalomba hozható és forgalmazható.
(6) A dohányzási célú gyógynövénytermékek gyártásában felhasznált összetevőkkel, azok mennyiségével, valamint az ezek változásával kapcsolatban a (3) és (4) bekezdés szerint benyújtott információkat az NNGYK a honlapján közzéteszi. A közzététel során a gazdasági szereplő által megjelölt üzleti titok védelmére tekintettel kell lenni.
18/D. § * A dohánytermékek és kapcsolódó termékek gyártói és importálói hiánytalan és helytálló információk közlésére kötelesek, a 18/B. § (1) bekezdésében meghatározott határidőn belül. A kért információk benyújtásának kötelezettsége elsődlegesen a gyártót terheli, ha a gyártó székhelye az Európai Unió valamely tagállamában található. A kért információk benyújtásának kötelezettsége elsődlegesen az importálót terheli, ha a gyártó székhelye az Európai Unión kívül, míg az importáló székhelye az Európai Unió valamely tagállamában található. A kért információk benyújtásának kötelezettsége a gyártót és az importálót közösen terheli, ha mindkettő székhelye az Európai Unión kívül van.
19. § * (1) * Az agrárpolitikáért felelős miniszter és az élelmiszerlánc-felügyeletért felelős miniszter a fogyasztók tájékoztatása érdekében a részére szolgáltatott valamennyi adatot az üzleti titok védelmére figyelemmel, az általa vezetett minisztérium internetes honlapján évente közzéteszi, továbbá a beérkezett adatokról tájékoztatást ad az egészségügyért felelős miniszter, az iparügyekért felelős miniszter és a fogyasztóvédelemért felelős miniszter számára.
(2) Az agrárpolitikáért felelős miniszter és az élelmiszerlánc-felügyeletért felelős miniszter az (1) bekezdésben meghatározott adatokat évente megküldi az Európai Bizottságnak.
19/A. § * (1) * Az Nvt. 7/D. § (1) bekezdése szerinti bejelentést a gyógyszerészeti államigazgatási szerv részére a 2015/2183 bizottsági végrehajtási határozat szerinti közös adatbeviteli kapun keresztül kell benyújtani magyar vagy angol nyelven, a 2015/2183 bizottsági végrehajtási határozat szerinti adattartalommal.
(1a) * Az (1) bekezdéstől eltérően a dohányzást helyettesítő nikotintartalmú termékek vonatkozásában az Nvt. 7/D. § (1) bekezdése szerinti bejelentést az országos tisztifőorvos részére az elektronikus ügyintézés és a bizalmi szolgáltatások általános szabályairól szóló törvény szerinti elektronikus úton kell megtenni.
(2) Az (1) bekezdés szerinti bejelentésnek a következő adatokat kell tartalmaznia:
a) a gyártó, importáló nevét és elérhetőségét,
b) a termék valamennyi összetevőjének, valamint a termék használata során keletkező kibocsátásoknak – és ezek mennyiségének – a felsorolását márkanevenként és típusonként,
c) toxikológiai adatokat a termék összetevőiről és a keletkező kibocsátásokról, elsődlegesen a belélegzés útján a fogyasztók, használók egészségére gyakorolt hatásukról, figyelembe véve esetleges függőséget okozó hatásukat,
d) információkat a rendeltetésszerű, illetve az ésszerűen előrelátható körülmények között történő fogyasztás esetén érvényes nikotindózisról és nikotinfelvételről,
e) a termék alkotórészeinek leírását, ideértve az elektronikus cigaretta, illetve az utántöltő flakon felbontásának és utántöltésének mechanizmusát,
f) a gyártási folyamat leírását – ezen belül kitérve arra, hogy a termék sorozatgyártott-e –, valamint nyilatkozatot arról, hogy a gyártási eljárás biztosítja a jogszabályokban foglalt követelményeknek való megfelelést, és
g) nyilatkozatot arról, hogy a gyártó és az importáló teljes felelősséget vállal a termék minőségéért és biztonságosságáért annak forgalomba hozatala és rendeltetésszerű, illetve ésszerűen előrelátható körülmények között történő felhasználása esetére.
(2a) * A (2) bekezdéstől eltérően a dohányzást helyettesítő nikotintartalmú termékek vonatkozásában a bejelentés tartalmára a 19/F. § (3) és (4) bekezdés rendelkezéseit kell alkalmazni.
(3) A termék minden olyan változtatása esetén, ami a (2) bekezdés szerinti adatokat érinti, új bejelentést kell benyújtani.
(4) A dohányzást imitáló elektronikus eszközök esetében a bejelentést a 2015/2183 bizottsági végrehajtási határozat szerinti közös adatbeviteli kapun keresztül a (2) bekezdés a)–c) és e)–g) pontja szerinti adattartalommal kell megtenni.
19/B. § * (1) Elektronikus cigaretta és utántöltő flakon a következő feltételekkel hozható forgalomba és forgalmazható:
a) nem tartalmazhat ízesítő anyagot,
b) * nikotintartalmú folyadék vagy bármilyen formában nikotint tartalmazó, elektronikus cigarettában és utántöltő flakonban használt folyadék kifejezetten erre a célra szolgáló,
ba) legfeljebb 10 ml űrtartalmú utántöltő flakonokban,
bb) legfeljebb 2 ml űrtartalmú eldobható elektronikus cigarettákban, patronokban vagy tartályokban hozható forgalomba.
c) a nikotintartalmú folyadék legfeljebb 20 mg/ml nikotint tartalmazhat,
d) a nikotintartalmú folyadék nem tartalmazhat
da) a 4. melléklet szerinti adalékanyagot,
db) vitaminokat vagy egyéb olyan adalékanyagokat, amelyek azt a benyomást keltik, hogy a terméknek kedvező élettani hatása van vagy az egészséget kevésbé veszélyezteti,
dc) koffeint, taurint vagy egyéb olyan adalékanyagokat és élénkítő hatású vegyületeket, amelyekhez az energikusság és a vitalitás képzete társul,
dd) a kibocsátásokat elszínező tulajdonságú adalékanyagokat,
de) az inhalációt vagy a nikotinfelvételt megkönnyítő adalékanyagokat, és
df) CMR tulajdonságokkal rendelkező adalékanyagokat,
e) a nikotintartalmú folyadék nem tartalmazhat 0,1%-nál több szennyeződést tartalmazó összetevőt,
f) a nikotintartalmú folyadék a 19/A. § (2) bekezdés b) pontja szerinti összetevőktől eltérő anyagokat csak nyomokban tartalmazhat, és csak abban az esetben használható fel, ha a nyomokban való előfordulás technikailag elkerülhetetlen a gyártás során,
g) a nikotin kivételével a nikotintartalmú folyadék kizárólag olyan összetevőkből állhat, amelyek – sem melegítés hatására, sem anélkül – nem veszélyesek az emberi egészségre,
h) az elektronikus cigaretták a nikotindózist rendes használati körülmények között egyenletesen adhatják le,
i) * az elektronikus cigarettákat és az utántöltő flakonokat gyermekbiztos zárral kell ellátni, és
j) az elektronikus cigarettákat és az utántöltő flakonokat védetté kell tenni törés és szivárgás ellen, valamint olyan mechanizmussal kell ellátni, amely garantálja a szivárgásmentes utántöltést.
(2) Az elektronikus cigaretták és az utántöltő flakonok csomagolási egységeihez tájékoztatót kell csatolni, amely a következőket tartalmazza:
a) a termék használati és tárolási útmutatóját – a használati útmutatóban utántöltési utasításokat és ábrákat –, valamint figyelemfelhívást arra, hogy a termék használata fiatalkorúak és nemdohányzók számára nem ajánlott,
b) az ellenjavallatokra vonatkozó tájékoztatást,
c) konkrét kockázati csoportoknak szóló figyelmeztetéseket,
d) a lehetséges káros hatásokra vonatkozó tájékoztatást,
e) a függőséget okozó tulajdonságokra és a toxicitásra vonatkozó tájékoztatást, és
f) a gyártó vagy az importáló, valamint a kapcsolattartó személy elérhetőségeit.
(3) Az elektronikus cigaretták és az utántöltő flakonok csomagolási egységein és gyűjtőcsomagjain fel kell tüntetni
a) a termékben található valamennyi összetevőt tömeg szerint csökkenő sorrendben,
b) a termék dózisonkénti nikotintartalmát és nikotinkibocsátását,
c) a gyártási tétel számát, és
d) a következő figyelmeztető feliratot: „A termék gyermekektől elzárva tartandó.
(4) Az elektronikus cigaretták és az utántöltő flakonok csomagolási egységeinek és gyűjtőcsomagjainak meg kell felelniük az Nvt. 6/A. § (1) bekezdés b), d) és e) pontjában, valamint (2) és (3) bekezdésében foglaltaknak.
(5) * A nikotintartalmú utántöltő folyadékkal előre megtöltött elektronikus cigaretták és az utántöltő flakonok csomagolási egységeinek és gyűjtőcsomagjainak két legnagyobb felületén, mindkét felületnek legalább a 30%-át kitöltő módon fel kell tüntetni a következő egészségvédő figyelmeztetést: „Ez a termék nikotint tartalmaz, amely erős függőséget okozó anyag.”
(6) Az (5) bekezdés szerinti egészségvédő figyelmeztetést fehér alapon, fekete színű, félkövér, Helvetica bold betűtípussal kell nyomtatni. A feliratot kisbetűvel kell szedni, kivéve a szöveg kezdőbetűjét, és azt az esetet, amikor a nagybetű használatát nyelvtani szabály követeli meg. Az egészségvédő figyelmeztetést a nyomtatására fenntartott területen középre zárva a csomag felső szélével párhuzamosan kell elhelyezni.
(7) * A gyógyszerészeti államigazgatási szerv a bejelentési kötelezettség teljesítéséről, valamint a bejelentett termék 19/A. és 19/B. §-nak való megfelelőségéről a hiánytalan bejelentés beérkezésétől – beleértve az igazgatási szolgáltatási díj beérkezését is – számított 60 napon belül igazolást állít ki.
19/C. § * (1) * Dohányzást imitáló elektronikus eszköz és nikotinmentes utántöltő flakon a következő feltételekkel hozható forgalomba és forgalmazható:
a) a bennük lévő folyadék nem tartalmazhat nikotint (a továbbiakban e § alkalmazásában: nikotinmentes folyadék),
b) a nikotinmentes folyadék nem tartalmazhat ízesítőanyagot,
c) a nikotinmentes folyadék nem tartalmazhat
ca) a 4. melléklet szerinti adalékanyagot,
cb) vitaminokat vagy egyéb olyan adalékanyagokat, amelyek azt a benyomást keltik, hogy a terméknek kedvező élettani hatása van, vagy az egészséget kevésbé veszélyezteti,
cc) koffeint, taurint vagy egyéb olyan adalékanyagokat és élénkítő hatású vegyületeket, amelyekhez az energikusság és a vitalitás képzete társul,
cd) a kibocsátásokat elszínező tulajdonságú adalékanyagokat,
ce) az inhalációt megkönnyítő adalékanyagokat és
cf) CMR tulajdonságokkal rendelkező adalékanyagokat, továbbá
cg) 0,1%-nál több szennyeződést tartalmazó összetevőt,
d) a nikotinmentes folyadék kizárólag olyan összetevőkből állhat, amelyek – sem melegítés hatására, sem anélkül – nem veszélyesek az emberi egészségre,
e) a termék gyermekbiztos zárral ellátott, és
f) a termék védett a törés és szivárgás ellen, valamint olyan mechanizmussal van ellátva, amely garantálja a szivárgásmentes utántöltést.
(2) A dohányzást imitáló elektronikus eszközök csomagolási egységeihez a 19/B. § (2) bekezdésében foglaltakat tartalmazó tájékoztatót kell csatolni.
(3) A dohányzást imitáló elektronikus eszköz csomagolási egységein és gyűjtőcsomagjain fel kell tüntetni
a) a termékben található valamennyi összetevőt tömeg szerint csökkenő sorrendben,
b) a gyártási tétel számát, és
c) a következő figyelmeztető feliratot: „A termék gyermekektől elzárva tartandó.
(4) A dohányzást imitáló elektronikus eszköz csomagolási egységeinek és gyűjtőcsomagjainak meg kell felelniük az Nvt. 6/A. § (1) bekezdés b), d) és e) pontjában, valamint (2) és (3) bekezdésében foglaltaknak.
(5) A dohányzást imitáló elektronikus eszköz csomagolási egységeinek és gyűjtőcsomagjainak két legnagyobb felületén, mindkét felületnek legalább a 30%-át kitöltő módon, a 19/B. § (6) bekezdésében foglaltaknak megfelelően fel kell tüntetni a következő egészségvédő figyelmeztetést: „Ez a termék dohányzást imitáló elektronikus eszköz. Használata gyermekek számára nem ajánlott.
(6) * A nikotinmentes utántöltő flakon csomagolási egységeinek és gyűjtőcsomagjainak két legnagyobb felületén, mindkét felületnek legalább a 30%-át kitöltő módon, a 19/B. § (6) bekezdésében foglaltaknak megfelelően fel kell tüntetni a következő egészségvédő figyelmeztetést: „Ez a termék nikotinmentes utántöltő flakon. Használata gyermekek számára tilos.”
19/D. § * (1) * Az elektronikus cigaretták, a dohányzást imitáló elektronikus eszközök és utántöltő flakonok, nikotinmentes patronok, valamint a nikotinmentes utántöltő flakonok gyártói és importálói kötelesek a közös adatbeviteli kapun keresztül évente adatokat szolgáltatni a tárgyévet követő év március 31-éig
a) márkanevenként és terméktípusonként az értékesítési volumenekről,
b) a különböző fogyasztói csoportok, köztük a fiatalkorúak, a nemdohányzók és a dohányzók főbb típusainak preferenciáiról,
c) a termékek értékesítési módjáról, és
d) az a)–c) pontban foglaltakkal kapcsolatosan végzett piackutatások összefoglalóiról, mellékelve azok angol fordítását is,
azzal, hogy a tárgyév a listák benyújtását megelőző év január 1-jétől december 31-éig tart.
(2) * A gyógyszerészeti államigazgatási szerv az (1) bekezdés szerinti adatokról más ország hatóságától is kérhet tájékoztatást, valamint más országok hatóságának megkeresésére a gyártók vagy importálók által rendelkezésre bocsátott adatokról tájékoztatást adhat. Az Európai Unión kívüli ország hatósága részére üzleti titoknak minősülő adat nem adható át.
(3) *
(4) * A gyógyszerészeti államigazgatási szerv az (1) bekezdés szerint szolgáltatott adatok alapján évente elemzést készít, és minden év május 31-éig megküldi az elemzését az egészségügyért felelős miniszternek. Az egészségügyért felelős miniszter által vezetett minisztérium az adatok alapján megvizsgálja, hogy az elektronikus cigaretta, a dohányzást imitáló elektronikus eszköz és az utántöltő flakonok használata nikotinfüggőséghez vezethet-e vagy dohánytermékek fogyasztására késztetheti-e a fiatalkorúakat és a nemdohányzókat.
(5) * Az (1) bekezdés szerint szolgáltatott adatokat és a (4) bekezdés szerint készült tájékoztatást a gyógyszerészeti államigazgatási szerv közzéteszi a honlapján az üzleti titok megsértése nélkül.
19/E. § * (1) Az elektronikus cigaretták és utántöltő flakonok gyártói, importőrei és forgalmazói kötelesek adatgyűjtési rendszert kialakítani és fenntartani ezen termékeknek az emberi egészségre gyakorolt valamennyi vélelmezett káros hatásáról.
(2) Ha a gyártó, az importőr vagy a forgalmazó bármelyike úgy véli, alapos okkal feltételezi, hogy a birtokában lévő, forgalomba hozni kívánt vagy forgalomba hozott termék nem biztonságos vagy nem jó minőségű, vagy más szempontból nem felel meg a vonatkozó jogszabályoknak, haladéktalanul megteszi az ahhoz szükséges korrekciós intézkedéseket, hogy az érintett termék megfeleljen az előírásoknak, illetve hogy azt kivonják a forgalomból vagy visszahívják. A termék gyártója, importőre vagy forgalmazója köteles azon tagállamok piacfelügyeleti hatóságait, ahol a terméket forgalmazzák vagy forgalmazni kívánják, haladéktalanul értesíteni elsősorban az emberi egészségre gyakorolt kockázatokról és biztonsági kockázatokról, valamint az esetlegesen megtett korrekciós intézkedésekről és azok eredményéről.
19/F. § * (1) A dohányzást helyettesítő nikotintartalmú termék legmagasabb nikotintartalma fogyasztási egységenként 17 mg.
(2) A dohányzást helyettesítő nikotintartalmú termék csomagolási egysége legfeljebb 20 darab terméket tartalmazó doboz.
(3) A dohányzást helyettesítő nikotintartalmú termék gyártói, importálói és forgalmazói kötelesek hat hónappal a tervezett forgalomba hozatalt megelőzően bejelentést tenni az országos tisztifőorvos részére elektronikus formában, a következő adattartalommal:
a) a gyártó, importáló, forgalmazó neve és elérhetősége,
b) a termék valamennyi összetevőjének, valamint az abból kioldódó anyagok és ezek mennyiségének felsorolása márkanevenként és típusonként,
c) toxikológiai adatok a termék összetevőiről,
d) nyilatkozat arról, hogy a gyártási eljárás biztosítja a jogszabályokban foglalt követelményeknek való megfelelést, és
e) nyilatkozat arról, hogy a gyártó, az importáló, illetve a forgalmazó teljes felelősséget vállal a termék minőségéért és biztonságosságáért annak forgalomba hozatala és rendeltetésszerű, illetve észszerűen előrelátható körülmények között történő felhasználása esetére.
(4) A termék minden olyan változtatása esetén, ami a (3) bekezdés szerinti adatokat érinti, új bejelentést kell benyújtani.
19/G. § * (1) Dohányzást helyettesítő nikotintartalmú termék akkor hozható forgalomba és forgalmazható, ha a termék nem tartalmaz
a) vitaminokat vagy egyéb olyan adalékanyagokat, amelyek azt a benyomást keltik, hogy a terméknek kedvező élettani hatása van vagy az egészséget kevésbé veszélyezteti,
b) koffeint, taurint vagy egyéb olyan adalékanyagokat és élénkítő hatású vegyületeket, amelyekhez az energikusság és a vitalitás képzete társul,
c) CMR tulajdonságokkal rendelkező adalékanyagokat,
d) 0,1%-nál több szennyeződést tartalmazó összetevőt.
(2) A termék csomagolási egységeihez tájékoztatót kell csatolni, amely tartalmazza:
a) a termék fogyasztási és tárolási útmutatóját, valamint figyelemfelhívást arra, hogy a termék használata fiatalkorúak számára tilos,
b) az ellenjavallatokra vonatkozó tájékoztatást,
c) konkrét kockázati csoportoknak szóló figyelmeztetéseket,
d) a lehetséges káros hatásokra vonatkozó tájékoztatást,
e) a függőséget okozó tulajdonságokra és a toxicitásra vonatkozó tájékoztatást és
f) a gyártó, forgalmazó vagy az importáló, valamint a kapcsolattartó személy elérhetőségeit.
(3) A termék csomagolási egységein és gyűjtőcsomagjain – az egyéb jogszabályban meghatározottakon túl – fel kell tüntetni
a) a termékben található valamennyi összetevőt tömeg szerint csökkenő sorrendben,
b) a termék fogyasztási egységenkénti nikotintartalmát,
c) a gyártási tétel számát és
d) a következő figyelmeztető feliratot jól látható, olvasható és letörölhetetlen módon: „A termék gyermekektől elzárva tartandó.”
(4) A (3) bekezdés szerinti figyelmeztető feliratot fehér alapon, fekete színű, félkövér, Helvetica bold betűtípussal kell nyomtatni. A feliratot kisbetűvel kell szedni, kivéve a szöveg kezdőbetűjét és azt az esetet, amikor a nagybetű használatát nyelvtani szabály követeli meg.
(5) A termék csomagolási egysége és a gyűjtőcsomagok címkézése, valamint maga a termék nem tartalmazhat olyan elemet vagy megoldást, amely
a) a terméket annak jellemzői, egészséghatásai, veszélyei vagy a kibocsátások tekintetében téves benyomást keltő módon reklámozza, illetve ilyen módon annak fogyasztására ösztönöz;
b) azt sugallja, hogy egy adott termék kevésbé káros, mint más termékek;
c) azt sugallja, hogy egy adott terméknek vitalizáló, energizáló, gyógyító, fiatalító, természetes, organikus jellemzői vannak, vagy más egészségügyi vagy életmódbeli előnyökkel jár;
d) ízre, illatra, ízesítőanyagra vagy más adalékanyagra, illetve ezek hiányára a fogyasztók megtévesztésére alkalmas módon utal;
e) élelmiszerre vagy kozmetikai termékre emlékeztet;
f) azt sugallja, hogy egyes termékek biológiai úton könnyebben lebomlanak, vagy más környezeti előnyökkel bírnak.
(6) A csomagolási egység és a gyűjtőcsomagok nem sugallhatnak gazdasági előnyt olyan kuponok alkalmazásával, amelyek kedvezményeket vagy ingyenes terjesztést kínálnak, illetve „egyet fizet, kettőt kap” vagy más hasonló jellegű ajánlatot tartalmaznak.
(7) A termék csomagolási egységeinek és gyűjtőcsomagjainak két, legnagyobb felületén mindkét felületnek legalább a 30%-át kitöltő módon fel kell tüntetni a következő egészségvédő figyelmeztetést: „Ez a termék nikotint tartalmaz, amely károsítja az ön egészségét, és függőséghez vezet.” Az egészségvédő figyelmeztetések nyomtatásának eltávolíthatatlannak, törölhetetlennek kell lennie a csomagolási egységeken és minden gyűjtőcsomagon, ideértve azt is, hogy azokat részben vagy egészen semmilyen formában nem takarhatja el, illetve nem zavarhatja meg semmilyen zárjegy, árcédula, biztonsági elem, csomagolóanyag, tasak, doboz vagy egyéb eszköz, amikor a termék forgalomba kerül.
(8) A (7) bekezdés szerinti egészségvédő figyelmeztetést fehér alapon, fekete színű, félkövér, Helvetica bold betűtípussal kell nyomtatni. A feliratot kisbetűvel kell szedni, kivéve a szöveg kezdőbetűjét és azt az esetet, amikor a nagybetű használatát nyelvtani szabály követeli meg. Az egészségvédő figyelmeztetést a nyomtatására fenntartott területen középre zárva, a csomag felső szélén kell elhelyezni.
(9) A termék csomagolási egységét gyermekbiztos zárral kell ellátni.
(10) Az országos tisztifőorvos a dohányzást helyettesítő nikotintartalmú termékekre vonatkozó bejelentések vizsgálatát követően – amennyiben a termék betiltása nem szükséges – a benyújtást követő 60 napon belül igazolást állít ki. Ha az országos tisztifőorvos 60 napon belül nem nyilatkozik, úgy a bejelentett termék forgalomba hozható és forgalmazható.
20. § (1) Ez a rendelet 2013. március 1-jén lép hatályba.
(2) Az e rendelet hatálybalépése előtt az Nvt. előírásainak megfelelően kihelyezett, de a 11. §-ban és a 7. mellékletben foglalt előírásoknak meg nem felelő feliratot vagy jelzést e rendelet hatálybalépésének napjától számított 12 hónapon belül kell a 11. §-ban és a 7. mellékletben foglalt előírásoknak megfelelően módosítani vagy cserélni.
(3) *
21. § A 2. §-ban és a 4. §-ban meghatározott technikai jellegű előírásoknak – a 2. § 6. pontjának a fogyasztói csomagolási egységre vonatkozó rendelkezése kivételével – nem kell megfelelnie azon dohánytermékeknek, amelyeket az Európai Unió valamely tagállamában vagy Törökországban állítottak elő, illetve hoztak forgalomba, vagy az Európai Gazdasági Térségről szóló megállapodásban részes valamely EFTA-államban állítottak elő, az ott irányadó előírásoknak megfelelően, feltéve, hogy az irányadó előírások az egészség védelme vonatkozásában az e rendeletben meghatározottal egyenértékű védelmet nyújtanak.
21/A. § * (1) * A 2016. május 19-én hatályos szabályoknak megfelelő dohányterméket – ha a (3)–(6) bekezdés eltérően nem rendelkezik –
a) 2016. december 31-éig lehet gyártani, importálni, bejegyzett kereskedő által fogadni,
b) 2017. február 28-áig lehet a dohány-kiskereskedelmi ellátó raktárába beszállítani,
c) 2017. május 20-áig lehet forgalomba hozni.
(2) A 2016. augusztus 20-a előtt gyártott vagy szabad kereskedelmi forgalomba helyezett dohányzási célú gyógynövénytermékek e rendelet 2016. augusztus 19-én hatályos rendelkezései szerint 2017. május 20-áig forgalomba hozhatók.
(3) * A dohánytermékek előállításáról, forgalomba hozataláról és ellenőrzéséről, a kombinált figyelmeztetésekről, valamint az egészségvédelmi bírság alkalmazásának részletes szabályairól szóló 39/2013. (II. 14.) Korm. rendelet módosításáról szóló 239/2016. (VIII. 16.) Korm. rendelettel (a továbbiakban: MódR.) megállapított 6/B. és 6/C. §-ban foglaltakat 2021. december 31-ig nem kell alkalmazni azon dohánytermékek esetében, amelyek 2016. április 30-áig az 1. melléklet szerinti adattartalommal a Nemzeti Fogyasztóvédelmi Hatóságnál vagy az ND Nemzeti Dohánykereskedelmi Nonprofit Zrt.-nél regisztrálásra kerültek, és azokon kizárólag a Jöt., az Nvt. és e rendelet 2016. május 19-ét követően hatályba lépett rendelkezéseiből (a továbbiakban együtt: irányelvet átültető rendelkezések) eredő változtatásokat hajtják végre. E termékek 2022. január 1-jétől már csak a MódR.-rel megállapított 6/B. és 6/C. § rendelkezéseinek megfelelő fogyasztói csomagolásban lehetnek forgalomban.
(4) * A MódR.-rel megállapított 6/B. és 6/C. §-ban foglaltakat
a) a 2016. április 30-át követően regisztrált és 2016. augusztus 19-ét követően forgalomba hozott új márkák és új alfajták esetében azonnal alkalmazni kell,
b) a 2016. április 30-át követően regisztrált és 2016. augusztus 20-át megelőzően forgalomba hozott új márkák és új alfajták esetében – ide nem értve a c) pont cb) alpontja szerinti termékeket – 2016. augusztus 19-ét követően alkalmazni kell akként, hogy legkésőbb 2018. május 20-án már csak a MódR.-rel megállapított 6/B. és 6/C. § rendelkezéseinek megfelelő fogyasztói csomagolásban lehetnek e termékek forgalomban,
c) azonnal alkalmazni kell
ca) a 2016. április 30-áig az 1. melléklet szerinti adattartalommal a Nemzeti Fogyasztóvédelmi Hatóságnál vagy az ND Nemzeti Dohánykereskedelmi Nonprofit Zrt.-nél regisztrálásra került azon dohánytermékek esetében vagy
cb) a 2016. április 30-át követően regisztrált és 2016. augusztus 20-át megelőzően forgalomba hozott új márkájú és új alfajtájú azon dohánytermékek esetében,
amelyeken nem kizárólag az irányelvet átültető rendelkezésekből eredő változtatásokat hajtanak végre.
(4a) * A (3) bekezdésben foglaltaktól eltérően 2022. január 1-jétől korlátlan ideig lehet forgalmazni a MódR.-rel megállapított 6/B. és 6/C. § rendelkezéseinek nem megfelelő, de egyébként a (3) bekezdésben foglalt véghatáridőt megelőzően hatályos jogszabályi rendelkezéseknek megfelelő fogyasztói csomagolásban lévő, a (3) bekezdés alá eső dohányterméket, feltéve, ha az a (3) bekezdésben foglalt véghatáridőt megelőzően a dohánytermék-kiskereskedőnél már készleten volt.
(5) * Mentol ízesítésű cigaretta és mentol ízesítésű cigarettadohány 2020. május 20-áig forgalmazható, azzal, hogy
a) a mentolos ízesítést a gyártási vagy csomagolási folyamat során kell a dohánytermékhez (annak bármely alkotórészéhez vagy a csomagolásához) hozzáadni, és
b) az ízesítés hozzáadása vagy adagolása részben sem függhet a fogyasztótól, így különösen nem lehet kapszulát alkalmazni a mentolos ízesítés hozzáadásához.
(6) Az (5) bekezdés a) és b) pontjában foglalt követelményeknek meg nem felelő mentol ízesítésű cigaretta és mentol ízesítésű cigarettadohány tekintetében az (1) bekezdésben foglaltak az irányadók.
(7) * A 2016. november 20-a előtt gyártott elektronikus cigaretták, utántöltő flakonok és dohányzást imitáló elektronikus eszközök 2017. május 20-áig hozhatók forgalomba.
(8) *
(9) * A 2016. május 19-én már forgalomban lévő elektronikus cigaretta, utántöltő flakon és dohányzást imitáló elektronikus eszközök esetében a MódR.-rel megállapított 19/D. § szerinti adatszolgáltatási kötelezettségnek első alkalommal 2017. december 31-éig kell eleget tenni.
(10) A MódR.-rel megállapított 18. § (1) bekezdése szerinti, a dohánytermékek összetevőire, valamint a kibocsátási szintekre vonatkozó információkat a 2016. augusztus 20-a előtt forgalomba hozott termékek esetén 2016. november 20-áig kell benyújtani.
(11) A MódR.-rel megállapított 18. § (2) bekezdése szerinti, az értékesítési volumenre vonatkozó adatokat első alkalommal 2016. november 20-áig kell benyújtani, azzal, hogy első alkalommal a 2015. január 1-jétől 2016. augusztus 20-áig tartó időszakra vonatkozóan kell adatot szolgáltatni.
(12) A MódR.-rel megállapított 18. § (6) bekezdése szerinti tanulmányokat, illetve összefoglalókat – ideértve a 2016. augusztus 20-át megelőzően készült tanulmányokat és összefoglalókat is – első alkalommal 2016. november 20-áig kell benyújtani.
(13) A MódR.-rel megállapított 7. § (1) bekezdés c) pontja 2019. május 20-áig azzal az eltéréssel alkalmazandó, hogy
a) * ha a zárjegyek, illetve az adózási célú nemzeti azonosító jelek kartonanyagból készült csomagolási egység felső szélén helyezkednek el, a hátsó felületre nyomtatandó kombinált egészségvédő figyelmeztetés elhelyezhető közvetlenül az adójegy, illetve azonosító jel alatt,
b) * ha a csomagolási egység puha anyagból készült, a csomag felső széle és a kombinált egészségvédő figyelmeztetés teteje között legfeljebb 13 mm magasságú, téglalap alakú felület maradjon a zárjegyek, illetve az adózási célú nemzeti azonosító jelek számára fenntartva,
c) álló tasakban forgalmazott fogyasztási dohány csomagolási egységén
ca) a kombinált egészségvédő figyelmeztetés az álló tasak első és hátsó felülete 65%-át foglalja el,
cb) a kombinált egészségvédő figyelmeztetés felső széle a felbontó csík alja, illetve – ha ilyen van – az annak eltávolítását szolgáló perforáció alatt, ahhoz közel helyezkedik el az álló tasakon úgy, hogy a kombinált egészségvédő figyelmeztetés ne sérüljön a tasak felbontásakor, és
cc) * a kombinált egészségvédő figyelmeztetés a tasak első oldalán – a nyomtatási tűréshatárokat figyelembe véve – a csomag teljes szélességében, míg hátsó, zárjegyet tartalmazó oldalán balra igazítva, a zárjegy számára a kombinált egészségvédő figyelmeztetés mellett jobbra helyet hagyva helyezkedik el.
(14) A MódR.-rel megállapított 18/C. § (1) bekezdése szerinti listát a 2016. augusztus 20-át megelőzően forgalomba hozott dohányzási célú gyógynövénytermékek összetevőire vonatkozóan 2016. november 20-áig kell benyújtani.
(15) * A MódR.-rel megállapított 8. § (1) bekezdése, valamint a 6/D. § (3) bekezdése szerinti év alatt első alkalommal a 2016. augusztus 20-ától 2017. december 31-éig tartó időszakot kell érteni, ezt követően év alatt a naptári évet kell érteni.
(16) A MódR.-rel megállapított 18/A. § (4) bekezdése szerinti jelentést első alkalommal 2018. július 1-jéig kell benyújtani.
(17) *
(18) * A 4/A. § (2) bekezdésében, valamint a 21/A. § (5) bekezdésében foglaltak maradéktalan érvényesülése érdekében 2017. május 20-át követően tilos az olyan szűrő, cigarettahüvely vagy más összetevő forgalmazása, amely kapszulát vagy más olyan megoldást tartalmaz, amellyel a fogyasztó a dohánytermékhez ízesítést adhat hozzá vagy adagolhat, függetlenül attól, hogy ezen összetevőkből és a dohány valamilyen formájából a dohányterméket a fogyasztó végső soron maga állíthatja elő.
(19) * Az irányelvet átültető rendelkezésekből eredő változtatások nem kimerítő felsorolását a 10. melléklet tartalmazza.
21/B. § * (1) E rendeletnek az egyes egészségügyi és egészségbiztosítási tárgyú kormányrendeletek módosításáról szóló 507/2017. (XII. 29.) Korm. rendelettel (a továbbiakban: MódR.3.) megállapított 6/A. § (3) bekezdésében, 6/D. § (2) bekezdés a) pontjában és 5. mellékletében foglaltakat – az e §-ban foglalt eltéréssel – 2018. május 1-től kell alkalmazni.
(2) A MódR.3.-mal megállapított 7. mellékletben foglalt előírásoknak meg nem felelő feliratot vagy jelzést 2019. december 31-ig kell módosítani vagy cserélni.
(3) A MódR.3.-mal megállapított 6/A. § (3) bekezdésében foglalt előírásoknak meg nem felelő általános figyelmeztetést legkésőbb 2018. július 1-ig kell módosítani vagy cserélni.
(4) A 2018. december 31-ét megelőzően gyártott és az egyéb jogszabályi feltételeknek megfelelő,
a) a 2. § 3. pont a) és e) alpontjában meghatározott dohánytermék a 21/A. § (3) és (4) bekezdésében meghatározottak szerinti időpontig, de legfeljebb 2019. május 19-ig,
b) az a) pont hatálya alá nem tartozó dohánytermék korlátlan ideig
forgalmazható akkor is, ha annak csomagolásán a „06 40 200 493”-as telefonszám szerepel.
21/C. § * (1) A 6/G. és 6/H. §-ban foglaltakat
a) a cigaretta és a cigarettadohány tekintetében 2019. május 20-tól,
b) a cigarettától és a cigarettadohánytól eltérő dohánytermékek tekintetében 2024. május 20-tól
kell alkalmazni.
(2) A 2019. május 20-a előtt az Európai Unióban gyártott vagy oda importált olyan cigaretta vagy cigarettadohány, amely nem tartalmazza a 6/G. § szerinti egyedi azonosítót, 2020. május 20-ig forgalmazható.
(3) A 2024. május 20-a előtt az Európai Unióban gyártott vagy oda importált olyan dohánytermék, amely nem minősül cigarettának vagy cigarettadohánynak, és amely nem tartalmazza a 6/G. § szerinti egyedi azonosítót, 2026. május 20-ig forgalmazható.
21/D. § * (1) E rendeletnek a dohánytermékek előállításáról, forgalomba hozataláról és ellenőrzéséről, a kombinált figyelmeztetésekről, valamint az egészségvédelmi bírság alkalmazásának részletes szabályairól szóló 39/2013. (II. 14.) Korm. rendelet jogharmonizációs célú módosításáról szóló 295/2023. (VII. 6.) Korm. rendelettel (a továbbiakban: MódR.4.) megállapított 4/A. § (5) bekezdésében, valamint 6/E. § (3) bekezdésében foglaltakat – a (2) bekezdésben foglalt eltéréssel – 2023. október 23-tól kell alkalmazni, azzal, hogy e szabályoknak meg nem felelő, de a dohánytermék-kiskereskedelmi tevékenységet végző személynél készleten lévő hevített dohánytermék korlátlan ideig forgalomba hozható.
(2) Az (1) bekezdéstől eltérően a MódR.4. hatálybalépése napján a fogyasztóvédelemért felelős miniszter által vezetett hatósági nyilvántartásban már regisztrált, a MódR.4. által megállapított 4/A. § (5) bekezdésében foglaltaknak meg nem felelő hevített dohányterméket a MódR.4. hatálybalépése napjától számított egy évig (a továbbiakban: véghatáridő) a dohány-kiskereskedelmi ellátó raktárába be lehet szállítani, és onnan – a véghatáridőig beszállított készlet kimerüléséig – a dohánytermék-kiskereskedelmi tevékenységet végző személy részére ki lehet szállítani. A dohánytermék-kiskereskedelmi tevékenységet végző személynél készleten lévő, e bekezdésnek megfelelően kiszállított hevített dohánytermék korlátlan ideig forgalomba hozható.
21/E. § * (1) A dohánytermékek előállításáról, forgalomba hozataláról és ellenőrzéséről, a kombinált figyelmeztetésekről, valamint az egészségvédelmi bírság alkalmazásának részletes szabályairól szóló 39/2013. (II. 14.) Korm. rendelet módosításáról szóló 120/2024. (VI. 10.) Korm. rendelet (a továbbiakban: MódR.5.) hatálybalépésekor már forgalomban lévő vagy az agrárpolitikáért felelős miniszternek korábban már bejelentett dohányzási célú gyógynövénytermékeket az e rendeletnek a MódR.5. által megállapított 18/C. §-a szerinti módon és adattartalommal 2024. december 31-ig kell az országos tisztifőorvosnak bejelenteni. Az e bekezdés szerinti bejelentési kötelezettség teljesítése során a 18/C. § (3) bekezdése szerinti hat hónapos határidő nem alkalmazandó.
(2) A (3) bekezdésben meghatározott kivétellel mindazon termékeket, amelyek a MódR.5. rendelkezéseinek nem felelnek meg, de megfelelnek az e rendeletnek a MódR.5. hatálybalépését megelőzően hatályos rendelkezéseinek, továbbá az egyéb hatályos és irányadó jogszabályoknak, az e rendelet hatálybalépésétől számított legfeljebb 1 évig lehet a dohánytermék-kiskereskedők részére forgalomba hozatal céljából átadni.
(3) * A (2) bekezdéstől eltérően mindazon dohányzást helyettesítő nikotintartalmú termékeket, amelyek az e rendeletnek a MódR.5. által megállapított 19/F. § (1) és (2) bekezdése, továbbá a 19/G. § (9) bekezdése rendelkezéseinek nem felelnek meg, de megfelelnek az e rendeletnek a MódR.5. hatálybalépését megelőzően hatályos rendelkezéseinek, továbbá az egyéb hatályos és irányadó jogszabályoknak, az e rendelet hatálybalépésétől számított legfeljebb 3 hónapig lehet a dohánytermék-kiskereskedők részére forgalomba hozatal céljából átadni.
(4) Mindazon termékeket, amelyek az e rendeletnek a MódR.5.-tel megállapított rendelkezéseinek nem felelnek meg, de megfelelnek az e rendeletnek a MódR.5. hatálybalépését megelőzően hatályos rendelkezéseinek, továbbá az egyéb hatályos és irányadó jogszabályoknak, és amelyeket a (2) és (3) bekezdés szerinti határidőig a dohánytermék-kiskereskedők készletre vették, a dohánytermék-kiskereskedők korlátlan ideig forgalomba hozhatják.
22. § A rendelet tervezetének a műszaki szabványok és szabályok terén történő információszolgáltatási eljárás megállapításáról és az információs társadalom szolgáltatásaira vonatkozó szabályok megállapításáról szóló 1998. június 22-i 98/34/EK európai parlamenti és tanácsi irányelv 8–10. cikkében előírt egyeztetése megtörtént.
23. § (1) * Ez a rendelet
a) a tagállamoknak a dohánytermékek és kapcsolódó termékek gyártására, kiszerelésére és értékesítésére vonatkozó törvényi, rendeleti és közigazgatási rendelkezései közelítéséről és a 2001/37/EK irányelv hatályon kívül helyezéséről szóló, 2014. április 3-i 2014/40/EU európai parlamenti és tanácsi irányelvnek,
b) a 2014/40/EU európai parlamenti és tanácsi irányelv II. mellékletének a dohánytermékeken feltüntetendő képes figyelmeztetéseket tartalmazó képtár létrehozása tekintetében történő módosításáról szóló, 2014. október 10-i 2014/109/EU bizottsági irányelvnek,
c) a dohányzásra szánt dohánytermékeken a kombinált egészségvédő figyelmeztetések elrendezésére, kialakítására és alakjára vonatkozó műszaki előírásokról szóló, 2015. október 9-i 2015/1842 EU bizottsági végrehajtási határozatnak,
d) a tasakban forgalmazott cigarettadohányon elhelyezendő általános figyelmeztetés és tájékoztatás pontos elhelyezéséről szóló, 2015. szeptember 24-i 2015/1735 bizottsági végrehajtási határozatnak,
e) az elektronikus cigarettákra és az utántöltő flakonokra vonatkozó értesítések közös formátumának meghatározásáról szóló, 2015. november 24-i 2015/2183 bizottsági végrehajtási határozatnak,
f) a dohánytermékekre vonatkozó információk benyújtása és nyilvános hozzáférhetővé tétele céljából alkalmazandó formátum meghatározásáról szóló, 2015. november 25-i 2015/2186 bizottsági végrehajtási határozatnak, és
g) az elektronikus cigaretták utántöltési mechanizmusára vonatkozó műszaki szabványokról szóló, 2016. április 14-i 2016/586 bizottsági végrehajtási határozatnak,
h) * a 2014/40/EU európai parlamenti és tanácsi irányelvnek a hevített dohánytermékekre vonatkozó egyes mentességek visszavonása tekintetében történő módosításáról szóló, 2022. június 29-i (EU) 2022/2100 felhatalmazáson alapuló bizottsági irányelvének
való megfelelést szolgálja.
(2) * Ez a rendelet az egyes műanyagtermékek környezetre gyakorolt hatásának csökkentéséről szóló (EU) 2019/904 európai parlamenti és tanácsi irányelv mellékletének D. részében felsorolt egyszer használatos műanyagtermékek harmonizált jelölésére vonatkozó szabályok megállapításáról szóló, 2020. december 17-i (EU) 2020/2151 bizottsági végrehajtási rendelet végrehajtásához szükséges rendelkezéseket állapít meg.
24. § * E rendeletnek a dohánytermékek előállításáról, forgalomba hozataláról és ellenőrzéséről, a kombinált figyelmeztetésekről, valamint az egészségvédelmi bírság alkalmazásának részletes szabályairól szóló 39/2013. (II. 14.) Korm. rendelet módosításáról szóló 421/2016. (XII. 14.) Korm. rendelettel (a továbbiakban: MódR.2.) megállapított rendelkezéseit a MódR.2. hatálybalépésekor folyamatban lévő eljárásokban is alkalmazni kell.
25. § * E rendeletnek a járási (fővárosi kerületi) hivatalok további megerősítésével összefüggő egyes kormányrendeletek módosításáról szóló 171/2017. (VI. 29.) Korm. rendelettel megállapított 11. § (2) és (4) bekezdésének hatálybalépése előtt megkezdett és a hatálybalépése időpontjában folyamatban lévő eljárásokat a 2017. június 30. napján hatályos rendelkezések szerint kell befejezni.
1. * Az adóraktár engedélyese, importáló vagy bejegyzett kereskedő neve, címe.
2. * A dohánytermék megnevezésére vonatkozó információk:
a) típusa [nem új dohánytermék-kategóriába tartozó termék esetén a 6. § (1) bekezdés a) pontja szerint]:
b) márkaneve/márkajelzése:
c) alfajtája (ha megkülönböztethető):
d) termékazonosítója (a 2015/2186 bizottsági végrehajtási határozat szerinti jelentési formátumban használt azonosító):
3. A dohánytermék
a) domináns dohánytartalma (például Virginia típusú, keleti típusú, Burley típusú), a felhasznált dohány géntechnológiával módosított / nem módosított,
b) összetevői, a felhasznált dohány-adalékanyagok funkcionális csoportonként (például természetes aroma, égésjavító),
c) mérete (mm)
ca) összes hosszúság (cigaretta, szivarka, szivar),
cb) vágatszélesség (fogyasztási dohány),
d) kémiai jellemzők
da) nikotintartalom (mg/cigaretta),
db) kátránytartalom (mg/cigaretta),
dc) szén-monoxid-tartalom (mg/cigaretta),
e) mennyiségi jellemzők
ea) a fogyasztói csomagolási egységben levő darabszám (cigaretta, szivar, szivarka),
eb) a fogyasztói csomagolási egységben levő termék tömege (fogyasztási dohány, rágásra vagy tüsszentésre szolgáló dohánytermék).
4. A füstszűrő alkalmazása.
5. A fogyasztói csomagolási egység grafikai és (teljes) szövegterve.
6. A fogyasztói, a gyűjtő- és a szállítási csomagolás módja.
Dátum: ......................................
.......................................................................
a dohányterméket előállító üzem vezetője,
importáló, bejegyzett kereskedő vagy tároló adóraktár engedélyes neve
1. Általános adatok
1.1. Az adalékanyag megnevezése, azonosító száma (E, CoE, FEMA, CAS)
1.2. Az adalékanyag pontos összetétele (természetes anyagok esetén elegendő az eredet és a gyártási mód megadása)
1.3. A gyártó neve és címe
1.4. A forgalomba hozó neve és címe
1.5. A tárolás módja, az adalékanyag eltarthatósági ideje
2. Fizikai-kémiai tulajdonságok
2.1. A hatóanyag(ok) kémiai és fizikai tulajdonságai (kémiai megnevezés, szerkezeti képlet, halmazállapot, szín, szag, oldhatóság, kémhatás stb.)
2.2. Az adalékanyag mikrobiológiai és kémiai tisztaságára és azonosságára vonatkozó adatok (hatóanyag-tartalom, melléktermékek és szennyezőanyagok megnevezése, mennyisége)
3. Az alkalmazásra vonatkozó adatok
3.1. Az adalékanyag rendeltetése (például nedvességmegtartó, égésjavító, aromaanyag)
3.2. Az anyag alkalmazásának technológiai indokolása
3.3. A felhasználás módja
3.4. Tervezett felhasználási koncentráció
4. Az adalékanyag ártalmatlanságát igazoló adatok, például JECFA értékelés, EC SCF állásfoglalás, aromaanyagok esetén FEMA GRAS, I.O.F.I. vagy CE listák
4/a. * Ha a 4. pont szerinti értékelések nem tartalmazzák, az adalékanyag és égéstermékeinek toxikológiai tulajdonságaira vonatkozó adatok, különös tekintettel a rákkeltő, valamint szívet, tüdőt és reprodukciót károsító hatásokra
5. Hazai gyártású adalékanyag vagy adalékanyag keverék esetén a gyártás technológiai leírása, a felhasznált anyagok tisztasága, keverék adalékanyag esetén az összetevők felsorolása, az adalékanyag-komponensek mennyisége
6. Az adalékanyag vizsgálatra alkalmas mennyiségű mintája
| CoE: | Council of Europe (Európa Tanács) | |
| FEMA | Flavor and Extract Manufacturers Association (Aroma és Extrakt Gyártók | |
| GRAS: | Egyesülése) GRAS = általában biztonságosnak elismert anyagok | |
| CAS: | Chemical Abstracts Service (Kémiai Referáló Szolgálat) | |
| JECFA: | Joint FAO/WHO Expert Committee on Food Additives (A FAO/WHO egyesített Élelmiszer Szakértői Bizottsága) | |
| EC SCF: | EC Scientific Committee on Food (az Európai Tanács Élelmiszer Tudományos Bizottsága) | |
| I.O.F.I.: | International Organization of the Flavour Industry (Aromaipari Nemzetközi Szervezet) |
| A | B | |
| Sorszám | Anyag | |
| 1 | 2-metil–3-(para-izopropil-fenil)propionaldehid | |
| 2 | Agar-agar | |
| 3 | Alumínium-oxid | |
| 4 | Ammónium-acetát | |
| 5 | Ammónium-citrát | |
| 6 | Ammónium-formiát | |
| 7 | Ammónium-hidrogén-karbonát | |
| 8 | Ammonium-hidrogén-malát | |
| 9 | Ammónium-hidroxid | |
| 10 | Ammónium-karbamát | |
| 11 | Ammónium-klorid | |
| 12 | Ammónium-laktát | |
| 13 | Ammónium-malát | |
| 14 | Ammónium-szukcinát | |
| 15 | Ammónium-szulfamát | |
| 16 | Ammónium-tartarát | |
| 17 | Antrakinonkék | |
| 18 | Bázikus kék 26 | |
| 19 | Borostyánkősav (E 363) | |
| 20 | Dehidro-mentho-furolakton | |
| 21 | Di–2-etil-hexil-adipát | |
| 22 | Diammónium-hidrogénfoszfát | |
| 23 | Diammónium-karbonát | |
| 24 | Diammónium-malát | |
| 25 | Diammónium-szukcinát | |
| 26 | Dibutil-ftalát | |
| 27 | Fenol-formaldehiddel módosított kolofónium | |
| 28 | Galaktóz | |
| 29 | Hangyasav (E 236) | |
| 30 | Karbamid (E 927b) | |
| 31 | Kárminvörös | |
| 32 | Krizein S | |
| 33 | Kumarinmentesített tonkabab | |
| 34 | Laktóz | |
| 35 | Maltóz | |
| 36 | Mannóz | |
| 37 | Metilibolya | |
| 38 | Méz | |
| 39 | Monoammónium-foszfát | |
| 40 | Nátrium-szilikát | |
| 41 | Oldószervörös 1 | |
| 42 | Pektinek | |
| 43 | Polietilén-glikol (E 1251) | |
| 44 | Riboflavin–5-foszfát | |
| 45 | Szacharóz-okta-acetát | |
| 46 | Szaharin (E 954) | |
| 47 | Szudánkék 11 | |
| 48 | Tea | |
| 49 | Theobromin | |
| 50 | Kannabidiol (CBD) | |
I. csoport
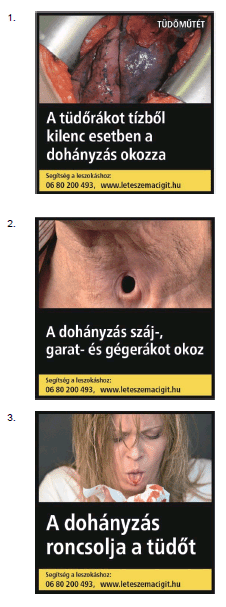
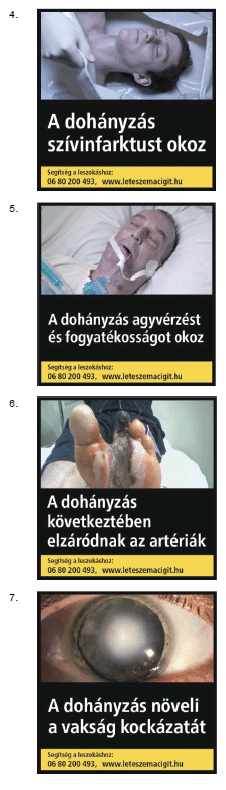


II. csoport




III. csoport
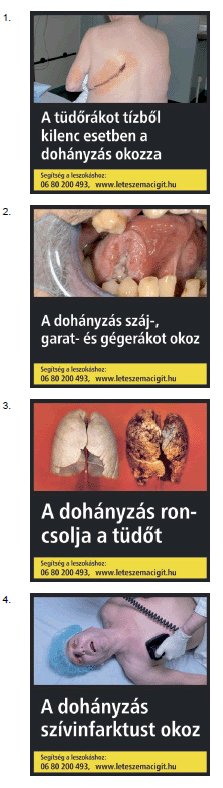
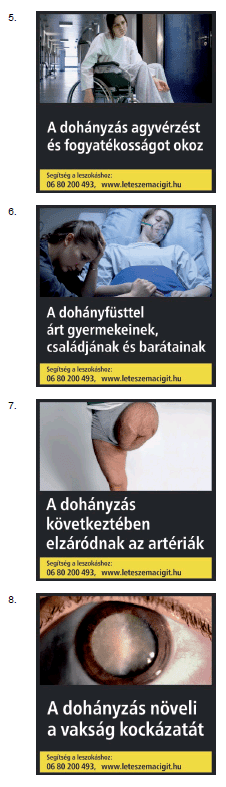


1.1. Ha a kombinált egészségvédő figyelmeztetés magassága nagyobb, mint a szélessége 70%-a, a gyártóknak a 4. pont 4.1. alpontjában található illusztrációnak megfelelően, egymás alatt kell elhelyezniük a figyelmezetés egyes elmeit.
1.2. Ha a kombinált egészségvédő figyelmeztetés magassága nagyobb, mint a szélessége 20%-a, de kisebb, mint a 65%-a, a gyártóknak a 4. pont 4.2. alpontjában található illusztrációnak megfelelően, egymás mellett kell elhelyezniük a figyelmezetés egyes elmeit.
1.3. Ha a kombinált egészségvédő figyelmeztetés magassága a szélességének legalább 65%-a, de legfeljebb 70%-a, a dohánytermékek gyártói maguk választhatják meg, hogy a figyelmeztetés egyes elemeit egymás alatt vagy egymás mellett rendezik el, feltéve, hogy a kombinált figyelmeztetés összes eleme teljesen látható marad és nem torzul.
1.4. Az elemek egymás alatti elrendezése esetén a fényképet a 4. pont 4.1. alpontjában található illusztrációnak megfelelően a kombinált egészségvédő figyelmeztetés felső részén, a figyelmeztető szöveg és a dohányzásról való leszokással kapcsolatos információ felett kell elhelyezni. A fénykép a külső fekete szegélyen belül a kombinált egészségvédő figyelmeztetés teljes felületének 50%-át, a szöveges figyelmeztetés a 38%-át, a dohányzásról való leszokással kapcsolatos információ pedig a 12%-át foglalja el.
1.5. Az elemek egymás melletti elrendezése esetén a fényképet a 4. pont 4.2. alpontjában található illusztrációnak megfelelően a kombinált egészségvédő figyelmeztetés bal felén, a szöveges figyelmeztetést a jobb felső, a dohányzásról való leszokással kapcsolatos információt pedig a jobb alsó részén kell elhelyezni. A fénykép a külső fekete szegélyen belül a kombinált egészségvédő figyelmeztetés teljes felületének 50%-át, a szöveges figyelmeztetés a 40%-át, a dohányzásról való leszokással kapcsolatos információ pedig a 10%-át foglalja el.
1.6. Ha a csomagolási egység vagy a gyűjtőcsomag alakja miatt a kombinált egészségvédő figyelmeztetés magassága a szélességének legfeljebb 20%-a, a kombinált egészségvédő figyelmeztetést a 4. pont 4.3. alpontjában található illusztrációnak megfelelő extra széles, egymás melletti elrendezésben kell feltüntetni. A fénykép a külső fekete szegélyen belül a kombinált egészségvédő figyelmeztetés teljes felületének 35%-át, a szöveges figyelmeztetés az 50%-át, a dohányzásról való leszokással kapcsolatos információ pedig a 15%-át foglalja el.
2.1. A kombinált egészségvédő figyelmeztetés nyomtatásánál a CMYK színrendszer négy színét kell használni. A fekete elemeknél a C0, M0, Y0 és K100, a napsárga elemeknél pedig a C0, M10, Y100 és K0 színkeveréket kell használni.
2.2. A kombinált egészségvédő figyelmeztetés minimális felbontása a valós méretben való nyomtatáskor 300dpi.
2.3. A szöveges figyelmeztetést fekete háttéren, fehér karakterekkel kell megjeleníteni. A dohányzásról való leszokással kapcsolatos információt – a 4. pontban található illusztrációknak megfelelően – napsárga háttéren, fekete karakterekkel kell megjeleníteni.
2.4. Ha az egyes elemeket egymás mellett, fordított sorrendben egymás alatt vagy egymás mellett extra széles formátumban rendezik el, a dohányzásról való leszokással kapcsolatos információs panelen belül egy 1 mm vastag fekete szegéllyel kell elválasztani a fényképet és az információ szövegét.
2.5. A gyártóknak és importőröknek gondoskodniuk kell arról, hogy a fényképet:
2.5.1. külön effektek alkalmazása, a színek kiigazítása, retusálás vagy a háttér megnövelése nélkül helyezzék a csomagolásra;
2.5.2. ne vágják ki a kép fókuszpontjához képest túl közel vagy túl távol; és
2.5.3. arányosan alakítsák át anélkül, hogy széthúznák vagy összenyomnák.
2.6. A gyártóknak biztosítaniuk kell, hogy:
2.6.1. a szöveges figyelmeztetés és a dohányzásról való leszokással kapcsolatos információ balra és függőlegesen középre legyen igazítva;
2.6.2. a szöveges figyelmeztetés és a dohányzásról való leszokással kapcsolatos információ megjelenítésénél a Neue Frutiger Condensed Bold betűtípust használják;
2.6.3. a szöveges figyelmeztetéshez egységes betűméretet használjanak;
2.6.4. a szöveg lehető legjobb láthatóságának biztosítása érdekében a szöveges figyelmeztetéshez és a dohányzásról való leszokással kapcsolatos információhoz szövegéhez a lehető legnagyobb betűméretet válasszák;
2.6.5. a szöveges figyelmeztetéshez és a dohányzásról való leszokással kapcsolatos információhoz használt betűméret legalább 6 pontos, illetve 5 pontos legyen;
2.6.6. a sortávolság 2 ponttal nagyobb legyen, mint a szöveges figyelmeztetés és 1–2 ponttal nagyobb, mint a dohányzásról való leszokással kapcsolatos információ betűmérete;
2.6.7. a szöveges figyelmeztetés – a nagybetűk használata tekintetében, de a számozástól eltekintve – az 5. mellékletben szereplő kombinált egészségvédő figyelmeztetéseken szereplő feliratokhoz igazodjon.
A 2.6.5. és a 2.6.6. ponttól eltérve, a cigarettától, a cigarettadohánytól és a vízipipadohánytól eltérő, dohányzásra szánt dohánytermékek gyártói és importőrei a kombinált egészségvédő figyelmeztetés egyes elemei teljes láthatóságának biztosítása mellett csökkenthetik a szöveges figyelmeztetés és a dohányzásról való leszokással kapcsolatos információ szövegénél használt betűtípus méretét és a sorok közötti távolságot, amennyiben ez elkerülhetetlen.
3.1. Az 1. pont 1.5. alpontjától eltérően a következő szabályok alkalmazandók a felhajtható (flip-top) fedelű csomagolási egységek elülső oldalán elhelyezendő kombinált egészségvédő figyelmeztetésekre:
a) abban az esetben, ha a csomagolási egység fedele kisebb, mint az 1. pont 1.5. alpontjában a fénykép elhelyezésére szánt felület, és a fenti előírásnak való megfelelés miatt a fedél felnyitása kettéosztaná a fényképet:
aa) a 4. pont 4.4. alpontjában található illusztrációnak megfelelően a szöveges figyelmeztetést a kombinált egészségvédő figyelmeztetés felső részén, a dohányzásról való leszokással kapcsolatos információ és a fénykép felett kell elhelyezni, valamint
ab) a fényképnek a külső fekete szegélyen belül a kombinált egészségvédő figyelmeztetés felületének legalább 50%-át, a szöveges figyelmeztetésnek legalább 30%-át és a dohányzásról való leszokással kapcsolatos információnak legalább 10%-át, de legfeljebb 12%-át kell elfoglalnia;
b) abban az esetben, ha a csomagolási egység fedele nagyobb, mint az 1. pont 1.5. alpontjában a fénykép elhelyezésére szánt felület, és a fenti előírásnak való megfelelés miatt a fedél felnyitása kettéosztaná a szöveges figyelmeztetést vagy a dohányzásról való leszokással kapcsolatos információt:
ba) a 4. pont 4.1. alpontjában található illusztrációnak megfelelően a fényképet a kombinált egészségvédő figyelmeztetés felső részén, a szöveges figyelmeztetés és a dohányzásról való leszokással kapcsolatos információ felett kell elhelyezni, valamint
bb) a fényképnek a külső fekete szegélyen belül a kombinált egészségvédő figyelmeztetés felületének legalább 50%-át, a szöveges figyelmeztetésnek legalább 30%-át és a dohányzásról való leszokással kapcsolatos információnak legalább 10%-át, de legfeljebb 12%-át kell elfoglalnia.
A gyártóknak gondoskodniuk kell arról, hogy a csomagolási egység felnyitása a kombinált egészségvédő figyelmeztetés három eleme közül egyiket se ossza ketté.
3.2. A 2. pont 2.6. alpont 2.6.5. és 2.6.6. pontjától eltérően a felhajtható (flip-top) fedelű csomagolási egységben forgalmazott cigaretta, cigarettadohány és vízipipadohány gyártói és importőrei a kombinált egészségvédő figyelmeztetés egyes elemei teljes láthatóságának biztosítása mellett csökkenthetik a csomagolás elülső oldalán található szöveges figyelmeztetés és dohányzásról való leszokással kapcsolatos információ szövegénél használt betűtípus méretét és a sorok közötti távolságot, ha a kombinált egészségvédő figyelmeztetést több nyelven is feltüntetik.
4.1. Egymás alatti elrendezés
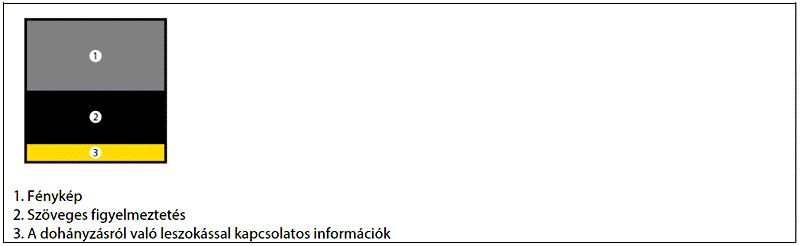
4.2. Egymás melletti elrendezés
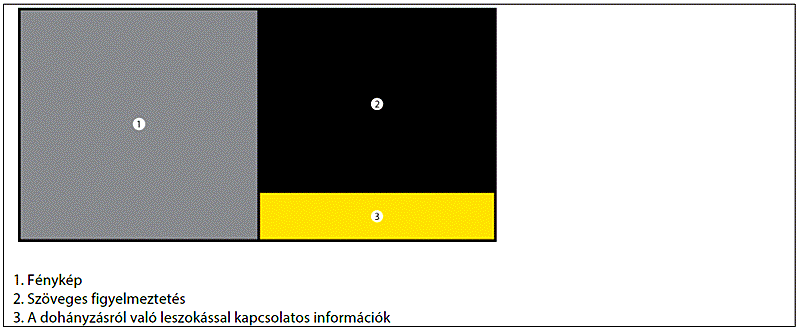
4.3. Egymás melletti elrendezés, extra széles formátum

4.4. Fordított egymás alatti elrendezés
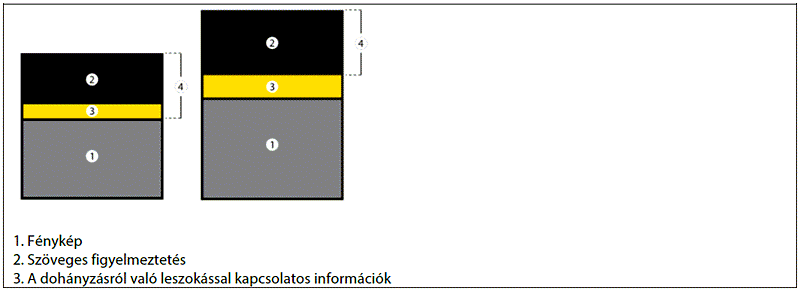

| A | B | ||
| 1. * | Bács-Kiskun Vármegyei Kormányhivatal | 10025004-00301181-00000000 | |
| 2. * | Baranya Vármegyei Kormányhivatal | 10024003–01040030–00000000 | |
| 3. * | Békés Vármegyei Kormányhivatal | 10026005–01040030–00000000 | |
| 4. * | Borsod-Abaúj-Zemplén Vármegyei Kormányhivatal | 10027006-00302852-00000000 | |
| 5. * | Csongrád-Csanád Vármegyei Kormányhivatal | 10028007-00302584-00000000 | |
| 6. * | Fejér Vármegyei Kormányhivatal | 10029008-00305350-00000000 | |
| 7. | Fővárosi Kormányhivatal | 10023002-00301253-00000000 | |
| 8. * | Győr-Moson-Sopron Vármegyei Kormányhivatal | 10033001-00301655-00000000 | |
| 9. * | Hajdú-Bihar Vármegyei Kormányhivatal | 10034002-00301954-00000000 | |
| 10. * | Heves Vármegyei Kormányhivatal | 10035003-00302113-00000000 | |
| 11. * | Jász-Nagykun-Szolnok Vármegyei Kormányhivatal | 10045002-00301947-00000000 | |
| 12. * | Komárom-Esztergom Vármegyei Kormányhivatal | 10036004-00304270-00000000 | |
| 13. * | Nógrád Vármegyei Kormányhivatal | 10037005-00302144-00000000 | |
| 14. * | Somogy Vármegyei Kormányhivatal | 10039007-00301129-00000000 | |
| 15. * | Szabolcs-Szatmár-Bereg Vármegyei Kormányhivatal | 10044001-00302285-00000000 | |
| 16. * | Tolna Vármegyei Kormányhivatal | 10046003-00306014-00000000 | |
| 17. * | Vas Vármegyei Kormányhivatal | 10047004-00301459-00000000 | |
| 18. * | Veszprém Vármegyei Kormányhivatal | 10048005-00301703-00000000 | |
| 19. * | Zala Vármegyei Kormányhivatal | 10049006-00303066-00000000 | |
| A | B | ||
| 1. | Országos Rendőr-főkapitányság | 10023002-01451715-30006009 | |
| 2. | Terrorelhárítási Központ | 10023002-00294267-30006009 | |
| 3. | Belügyminisztérium Országos Katasztrófavédelmi Főigazgatóság | 10023002-00283494-30006009 | |
| 4. | Büntetés-végrehajtás Országos Parancsnoksága | 10023002-01393008-30006009 | |
| 5. | Magyar Honvédség Közegészségügyi Járványügyi Szolgálat | a bírságot kiszabó határozatban megjelölt, a Magyar Honvédség Közegészségügyi Járványügyi Szolgálat Magyar Államkincstárnál vezetett egészségügyi bírság és egészségvédelmi bírság befizetési számlája | |
1. MSZ ISO 4387
Cigaretták. Az összes és a nikotinmentes száraz részecskefázis meghatározása rutinanalitikai cigaretta-elszívató gép alkalmazásával
2. MSZ ISO 8243
Cigaretták. Mintavétel
3. MSZ ISO 10315
Cigaretták. A nikotintartalom meghatározása füstkondenzátumokban. Gázkromatográfiás módszer
4. MSZ ISO 10362–1
Cigaretták. A víz meghatározása füstkondenzátumokban. 1. rész: Gázkromatográfiás módszer, vagy
5. MSZ ISO 10362–2
Cigaretták. A víz meghatározása füstkondenzátumokban. 2. rész: Karl Fischer-módszer
6. MSZ ISO 8454
Cigaretták. A szén-monoxid meghatározása a cigarettafüst gőzfázisában. NDIR módszer
7. MSZ EN ISO 12863:2010
A cigaretták tűzokozó hatásának értékelése szabványos vizsgálati módszerrel
8. MSZ EN 16156:2011
Cigaretták. A tűzokozó hatás értékelése. Biztonsági követelmények
A 21/A. § értelmezésében az irányelvet átültető rendelkezésekből eredő változtatásoknak különösen a következők minősülnek:
1. A dohánytermék csomagolásának az e rendelet által meghatározott egészségvédő figyelmeztetésekkel le nem fedett felületein a Nemzeti Fogyasztóvédelmi Hatóságnál vagy az ND Nemzeti Dohánykereskedelmi Nonprofit Zrt.-nél
a) 2016. április 30-áig regisztrált vagy
b) 2016. április 30-át követően, de 2016. augusztus 19-éig a 2016. május 19-én hatályos jogszabályok szerinti regisztrációra benyújtott és ugyancsak 2016. augusztus 19-éig forgalomba hozott
dohánytermékek csomagolásán szereplő olyan elemek (szövegek, ábrák és jellemző színvilág) szerepeltetése a rendelkezésre álló felülethez igazítva, amely elemek nem sértik az e rendeletben, az Nvt.-ben vagy a Jöt.-ben kifejezetten megállapított bármely tilalmat.
Az e pontban meghatározott elemek elhelyezésére rendelkezésre álló felületekhez igazítása során az egyes elemek bármelyike elhagyható, az egyes elemek mérete (beleértve egyes elemek méretének növelését), előfordulási száma (beleértve annak növelését), egymáshoz és a csomagoláshoz viszonyított elhelyezkedése, valamint aránya megváltoztatható, továbbá az egyes elemeken olyan változtatások is végrehajthatóak, amelyek révén az elemek jobban illenek a rendelkezésre álló megváltozott felülethez.
2. Ha a dohánytermék márkaneve, alfajtaneve vagy csomagolása tartalmazza a „Slim”, „Slims”, „Superslim”, „Superslims”, „Demislim” vagy „Demislims” szavakat vagy valamely szót, illetve más elemet, amely az Nvt. 6/A. §-ában foglaltakkal ellentétes lehet, akkor
a) a márkanévből, az alfajtanévből, illetve a csomagolásból az itt említett szó, illetve elem kivétele, és egyúttal
b) olyan új alfajta név, szó, illetve csomagolási elem feltüntetése a csomagoláson, amely megfelel e rendelet és az Nvt. előírásainak.
3. Ha a dohánytermék márkaneve vagy alfajtaneve az Nvt. 6/A. § (1) bekezdés a) pontjában foglaltak ellenére a dohánytermék nikotin-, kátrány-, illetve szén-monoxid-tartalmára vonatkozó információt tartalmaz, akkor
a) a márkanévből, illetve az alfajtanévből a dohánytermék nikotin-, kátrány-, illetve szén-monoxid-tartalmára vonatkozó információt tartalmazó rész kivétele és egyúttal
b) olyan új alfajtanév feltüntetése a csomagoláson, amely név nem tartalmaz a dohánytermék nikotin-, kátrány-, illetve szén-monoxid-tartalmára vonatkozó információt, és egyébként megfelel e rendelet és az Nvt. előírásainak.
4. Mentol ízesítésű dohánytermékek esetében a „mentol” szó feltüntetése a csomagoláson.
5. Ha a dohánytermék ízesített kapszulát tartalmaz, akkor
a) a kapszula eltávolítása a dohánytermékből,
b) a csomagoláson lévő, a termék kapszulás voltára utaló feliratok és ábrák eltávolítása vagy átalakítása akként, hogy azok ne tartalmazzanak utalást kapszulára,
c) – ha az eltávolított felirat a termék alfajtanevének része volt – olyan alfajtanév feltüntetése a csomagoláson, amely név nem tartalmaz utalást kapszulára, és egyébként megfelel e rendelet és az Nvt. előírásainak,
d) – ha a termék mentolos ízesítésű kapszulát (is) tartalmazott – a termék e rendelet által megengedett módon történő ellátása mentol ízesítéssel, továbbá – ha mentoltól eltérő ízt is tartalmazó kapszulás termékről van szó – az egyéb ízesítésre utaló megjelölések, ábrák, színek eltávolítása vagy megváltoztatása annak érdekében, hogy azok kizárólagosan a mentolos ízesítésre utaljanak.
6. A dohánytermékek kiszerelésének (tömeg, darabszám) megváltoztatása, új kiszerelés alkalmazása annak érdekében, hogy
a) az ennél kevesebb szálat tartalmazó cigaretta egységcsomagja 20 szálasra változzék, vagy
b) a cigarettadohány 30–50 grammos kiszerelésűre változzék akkor, ha korábban 50 grammnál nagyobb kiszerelésben volt elérhető az adott termék.
7. * A 2–6. pontban felsorolt esetekben az érintett dohánytermék új csomagolásának a fogyasztóvédelemért felelős miniszter felé történő regisztrációja során a regisztrációs laphoz fűzött külön megjegyzésben a regisztrációs lapot benyújtó köteles megindokolni, hogy milyen okból vált szükségessé a dohánytermék márkanevének, illetve alfajtanevének megváltoztatása.